题目内容
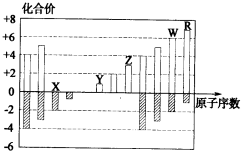
如图所示是五种短周期元素化合价与原子序数的关系,有关说法不正确的是( )

| A、原子半径:R>W>Z>Y>X |
| B、五种原子的核外最外层电子数总和为23 |
| C、X与Y可形成既含离子键又含共价键的化合物 |
| D、X、Y、W可能形成水溶液呈碱性的化合物 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X只有负化合价和0价,且负化合价为-2价,则为O元素,Y只有0价和+1价,且原子序数大于X,则Y为Na元素,同理,Z为Al元素、W为S元素、R为Cl元素,
A.原子的电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数的增大而减小;
B.根据其最外层电子数计算;
C.X和Y形成的化合物有Na2O、Na2O2;
D.X、Y、W可能形成化合物为Na2SO4、Na2SO3.
A.原子的电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数的增大而减小;
B.根据其最外层电子数计算;
C.X和Y形成的化合物有Na2O、Na2O2;
D.X、Y、W可能形成化合物为Na2SO4、Na2SO3.
解答:
解:X只有负化合价和0价,且负化合价为-2价,则为O元素,Y只有0价和+1价,且原子序数大于X,则Y为Na元素,同理,Z为Al元素、W为S元素、R为Cl元素,
A.原子的电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数的增大而减小,原子半径:Y>Z>W>R>X,故A错误;
B.其最外层电子数之和=6+1+3+6+7=23,故B正确;
C.X和Y形成的化合物有Na2O、Na2O2,过氧化钠中存在离子键和非极性键,故C正确;
D.X、Y、W可能形成化合物为Na2SO4、Na2SO3,亚硫酸钠是强碱弱酸盐,亚硫酸根离子水解导致溶液呈碱性,故D正确;
故选A.
A.原子的电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数的增大而减小,原子半径:Y>Z>W>R>X,故A错误;
B.其最外层电子数之和=6+1+3+6+7=23,故B正确;
C.X和Y形成的化合物有Na2O、Na2O2,过氧化钠中存在离子键和非极性键,故C正确;
D.X、Y、W可能形成化合物为Na2SO4、Na2SO3,亚硫酸钠是强碱弱酸盐,亚硫酸根离子水解导致溶液呈碱性,故D正确;
故选A.
点评:本题考查了原子结构和元素周期律,根据题干中元素化合价确定元素,再结合物质结构、性质结合元素周期律解答,注意CD中化合物多种,为易错点.

练习册系列答案
相关题目
为提纯下列物质(括号内为杂质),所选试剂及方法均正确的是( )
| 选项 | 物质 | 除杂试剂 | 方法 |
| A | 溴苯(溴) | CCl4 | 分液 |
| B | NH3(H2O) | 浓硫酸 | 洗气 |
| C | 乙烷(乙烯) | 溴水 | 洗气 |
| D | CO2(SO2) | Na2CO3饱和溶液 | 洗气 |
| A、A | B、B | C、C | D、D |
下列排列顺序正确的是( )
| A、热稳定性强弱:HCl>HBr>HI |
| B、微粒半径:Cl->K+>Na+>Fe(OH)3胶粒 |
| C、晶体熔点:SiO2>NaCl>CF4>CCl4 |
| D、氢化物的沸点:H2Se>H2S>H2O |
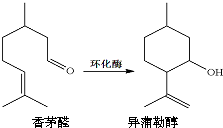 香茅醛是一种食用香精,异蒲勒醇是一种增香剂,一定条件下,香茅醛可转化为异蒲勒醇.下列说法不正确的是( )
香茅醛是一种食用香精,异蒲勒醇是一种增香剂,一定条件下,香茅醛可转化为异蒲勒醇.下列说法不正确的是( )| A、香茅醛与异蒲勒醇互为同分异构体 |
| B、香茅醛的分子式为C10H19O |
| C、异蒲勒醇可发生加成、取代、消去反应 |
| D、鉴别香茅醛与异蒲勒醇可用Br2水 |
下列物质中,S元素的化合价为+6的是( )
| A、S |
| B、H2SO4 |
| C、SO2 |
| D、H2S |
下列反应中,属于取代反应的是( )
| A、乙醇在一定条件下与氧气反应生成乙醛 |
| B、苯的硝化反应 |
| C、乙烯在一定条件下生成聚乙烯 |
| D、乙烯与溴的四氯化碳溶液反应 |
NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、1mol乙烷(CH3CH3)中含有共价键的数目为6NA |
| B、由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA |
| C、标准状况下,22.4L H2O中含氢原子数为2NA |
| D、制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为NA |
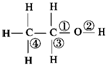 乙醇在一定条件下,发生催化氧化反应时,化学键断裂位置是图中的( )
乙醇在一定条件下,发生催化氧化反应时,化学键断裂位置是图中的( )| A、②③ | B、②④ | C、①③ | D、③④ |