题目内容
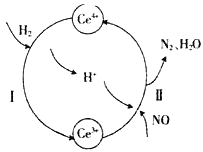
【题目】用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx),转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其转化过程如下图所示。下列说法不正确的是
A. 反应I的离子反应方程式为2Ce4++H2=2Ce3++2H+
B. 反应II中氧化剂与还原剂的物质的量之比为1:2
C. 反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+)
D. 反应过程中混合溶液内Ce3+和Ce4+离子的总数一定保持不变
【答案】C
【解析】
A.根据图示可知反应I为2Ce4++H2=2Ce3++2H+,A正确;
B.反应II的反应物为Ce3+、H+、NO,生成物为Ce4+、N2、H2O,根据电子守恒、电荷守恒及原子守恒,可得反应方程式为 4Ce3++4H++2NO=4Ce4++N2+2H2O,在该反应中NO是氧化剂,Ce3+是还原剂,故氧化剂与还原剂的物质的量的比为2:4=1:2,B正确;
C.反应前后溶液中n(Ce4+)的物质的量不变,但由于反应后溶液中水的物质的量增多,所以反应后溶液中c(Ce4+)减小,C错误;
D.由于反应前后各种元素的原子个数相等,根据Ce元素守恒可知反应过程中混合溶液内Ce3+和Ce4+离子的总数不变,D正确;
故合理选项是C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目