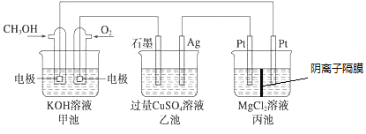
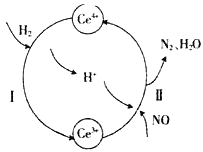
题目内容
【题目】常温下氨能被Cl2、Br2等氧化,已知以下反应:8NH3+3Cl2→6NH4Cl+N2。
(1)用单线桥标出电子转移的方向和数目______。
(2)这一反应中,氧化剂是______,氧化产物是______。
(3)若有3mol N2生成,则发生氧化反应的物质有______mol
(4)根据上述反应,若将浓氨水与Cl2靠近,将会看到______(现象)。
【答案】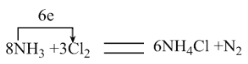 氯气 氮气 6mol 有白烟生成
氯气 氮气 6mol 有白烟生成
【解析】
反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,氨气作还原剂,氯气作氧化剂;据此解答。
(1)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为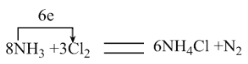 ;
;
(2)反应8NH3+3Cl2=6NH4Cl+N2中,氧化剂是氯气,氧化产物是氮气,故答案为:Cl2;N2;
(3)若有3molN2生成,则发生氧化反应的氨气为6mol,故答案为:6mol;
(4)反应8NH3+3Cl2=6NH4Cl+N2中,所以将浓氨水与Cl2靠近,有NH4Cl固体生成,将会产生大量的白烟,故答案为:白烟。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目