题目内容
1.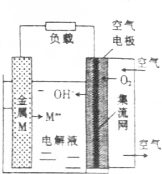 2014年亚待兰大先进汽车电池会议上,美铝公司(A1coa)与以色空气列phnergy公司提出联合开发phinergy铝-空气电池.铝-空气电池属于金属燃料电池的一种,常见金属燃料电池的结构如图空气所示.下列说法不正确的是( )
2014年亚待兰大先进汽车电池会议上,美铝公司(A1coa)与以色空气列phnergy公司提出联合开发phinergy铝-空气电池.铝-空气电池属于金属燃料电池的一种,常见金属燃料电池的结构如图空气所示.下列说法不正确的是( )| A. | 电池工作时,电子沿金属M→负载→空气电极流动 | |
| B. | 若M为Al,电解液为NaC1溶液.则电池工作一段时间后.电解液的pH增大 | |
| C. | 若M为Mg.电解液为NaCl溶液,则电池的总反应方程式为2Mg+O2+2H2O═2Mg(OH)2 | |
| D. | 集流网可增大接触面,从而吸附更多的氧气,提高金属电池的工作效率. |
分析 根据金属燃料电池的结构图,可以看出金属M为负极失电子发生氧化反应,空气电极为正极得电子发生还原反应,电池工作时,电子负极→正极,电池的总反应方程式即为自发的氧化还原反应,据此分析.
解答 解:A.金属燃料电池的结构图,可以看出金属M为负极失电子发生氧化反应,空气电极为正极得电子发生还原反应,所以电子沿金属M→负载→空气电极流动,故A正确;
B.若M为Al,电解液为NaC1溶液,电池总反应为4Al+3O2+6H2O=4Al(OH)3,所以电池工作一段时间后.电解液的pH不变,故B错误;
C.若M为Mg.电解液为NaCl溶液,则电池的总反应方程式为2Mg+O2+2H2O═2Mg(OH)2,故C正确;
D.集流网可增大接触面,从而吸附更多的氧气,则可以提高金属电池的工作效率,故D正确;
故选B.
点评 本题考查原电池原理,明确电极上得失电子及反应是解本题关键,难度不大,注意电池的总反应方程式的书写.

练习册系列答案
相关题目
11.已知次氯酸是比碳酸还弱的酸,反应Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增大,H+浓度减小,可加入( )
| A. | Na2SO3固体 | B. | 水 | C. | CaCO3固体 | D. | NaOH固体 |
12.下列叙述中正确的是( )
| A. | ${\;}_{17}^{37}$Cl的中子数为37 | B. | H2O与D2O互称同素异形体 | ||
| C. | NH3的电子式为 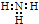 | D. | 1H与D互称同位素 |
9.H2有还原性,可以还原氧化铜,是因为H2中氢元素的化合价处于低价(0价),可以升高至+1价.由此分析:下列化学反应的反应物中的氢元素能体现还原性的是( )
| A. | Mg+2HCl═MgCl2+H2↑ | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | NaH+H2O═NaOH+H2↑ | D. | 2H2O2═2H2O+O2↑ |
16.离子方程式Ba2++SO42-═BaSO4↓可表示下列反应中的:
①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应
②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应
③稀硫酸与可溶性钡盐溶液之间的反应
④氢氧化钡溶液与稀硫酸反应.
说法正确的是( )
①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应
②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应
③稀硫酸与可溶性钡盐溶液之间的反应
④氢氧化钡溶液与稀硫酸反应.
说法正确的是( )
| A. | ①② | B. | ①②④ | C. | ②③ | D. | ①③ |
6.下列物质中存在的化学键,在熔化时没有破坏的是( )
| A. | 金属铜 | B. | 碘 | C. | 固体氮 | D. | 硫酸钠 |
13.关于对用惰性电极电解CuCl2溶液过程中的现象及本质的分析中正确的是( )
| A. | 所用电源可以直流电也可以是交流电 | |
| B. | 电解池工作过程中,阴离子移向阴极,阳离子移向阳极区 | |
| C. | 阳极区产生的气体可使湿润的KI-淀粉试纸变蓝色 | |
| D. | 若不考虑产物Cl2溶解产生的影响,则电解过程中溶液的浓度保持不变. |