题目内容
【题目】某学习小组设计实验探究CuSO4分解产物
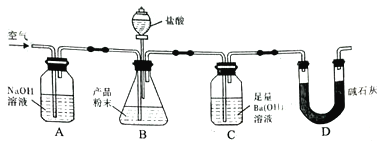
Ⅰ.甲同学选择下列装置设计实验探究硫酸铜分解的气态产物SO3、SO2和O2,并验证SO2的还原性。
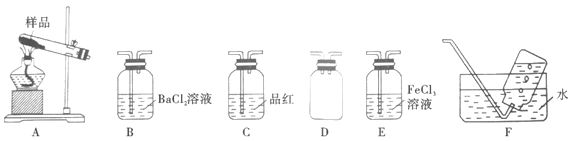
回答下列有关问题
(1)CuSO4水溶液呈酸性,其原因是______________________(用离子方程式表示)。
(2)上述装置按气流从左至右排序为A、D、___________E、F(填代号)。
(3)装置D的作用是___________;能证明有SO3生成的实验现象是___________。
(4)在实验过程中C装置中红色溶液逐渐变为无色溶液,说明A中分解产物有___________;待C中有明显现象后,F开始收集气体,F装置中集气瓶收集到了少量气体,该气体是___________(填化学式)。
(5)为了验证SO2的还原性,取E装置中反应后的溶液于试管中,设计如下实验:
a 滴加少量的NH4SCN溶液 b 滴加少量的K3[Fe(CN)6]溶液
c 滴加酸性KMnO4溶液 d 滴加盐酸酸化的BaCl2溶液
其中,方案合理的有___________(填代号),写出E装置中可能发生反应的离子方程式:_________。
Ⅱ.乙同学利用A中残留固体验证固体产物(假设硫酸铜已完全分解)
查阅资料知,铜有+2、+1价。Cu2O在酸性条件下不稳定,发生反应:Cu2O+2H+=Cu+Cu2++H2O。
(6)为了验证固体产物中是否有Cu2O,设计了下列4种方案,其中能达到实验目的的是___________。
甲:取少量残留固体于试管,滴加足量的稀硝酸,观察溶液颜色是否变为蓝色
乙:取少量残留固体于试管,滴加足量的稀硫酸,观察溶液颜色是否变为蓝色
丙:取少量残留固体于试管,滴加足量的稀盐酸,观察是否有红色固体生成
丁:取少量残留固体于试管,通入氢气,加热,观察是否生成红色固体
(7)经检验CuSO4分解生成CuO、Cu2O、SO3、SO2和O2,且CuO、Cu2O的质量之比为5:9,SO2、O2、SO3的体积之比(同温同压下测定)为4:3:2。写出CuSO4分解的化学方程式:_______。
【答案】![]() B、C 防倒吸(或作安全瓶) B装置中产生白色沉淀 SO2 O2 bd
B、C 防倒吸(或作安全瓶) B装置中产生白色沉淀 SO2 O2 bd ![]() 乙
乙 ![]()
【解析】
装置A中CuSO4受热分解,装置D为安全瓶,起防止倒吸的作用,装置B中氯化钡溶液用于检验分解产物中是否有三氧化硫,装置C中品红溶液用于检验分解产物中是否有二氧化硫,装置E中氯化铁溶液用于验证二氧化硫的还原性,装置F用于检验分解产物中是否有难溶于水的氧气。
(1)CuSO4是强酸弱碱盐,Cu2+在溶液中水解,使溶液呈酸性,收集到离子方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)三氧化硫与水剧烈反应生成强酸硫酸,为防止倒吸应在检验三氧化硫前设计一个防倒吸的装置,二氧化硫部分与水反应生成弱酸亚硫酸,由强酸制弱酸的原理可知,三氧化硫能与氯化钡溶液反应生成硫酸钡白色沉淀,二氧化硫不能与氯化钡溶液反应,为防止三氧化硫干扰实验,应先检验三氧化硫,再检验二氧化硫,检验二氧化硫用品红溶液,验证二氧化硫的还原性用氯化铁溶液,验证氧气可用排水法,则连接顺序为A、D、B、C、E、F,故答案为:B、C;
(3)三氧化硫与水剧烈反应生成强酸硫酸,为防止倒吸应在检验三氧化硫前设计一个防倒吸的装置,则装置D的作用是做安全瓶,起防止倒吸的作用;三氧化硫能与氯化钡溶液反应生成硫酸钡白色沉淀,二氧化硫不能与氯化钡溶液反应,故答案为:防倒吸(或作安全瓶);B装置中产生白色沉淀;
(4)二氧化硫具有漂白性,能使品红溶液褪色,C装置中品红溶液红色溶液逐渐变为无色溶液,说明A中分解产物有二氧化硫,则反应中S元素的化合价降低,又因为Cu元素的化合价不可能升高,故只能是O元素的化合价升高生成氧气,且氧气难溶于水,能用排水集气法收集,则F装置中集气瓶收集到的少量气体是氧气,故答案为:SO2;O2;
(5)二氧化硫具有漂白性,氯化铁具有氧化性,二氧化硫与氯化铁溶液发生氧化还原反应生成硫酸、氯化亚铁,反应的离子方程式为![]() ,为验证二氧化硫的还原性,可以检验E中的溶液中是否有Fe2+或SO42-生成。NH4SCN溶液不能检验这两种离子;亚铁离子能与K3[Fe(CN)6]溶液生成蓝色沉淀;Cl-也有还原性,故不能用酸性KMnO4溶液检验Fe2+;盐酸酸化的BaCl2溶液可以检验SO42-,则检验反应生成的亚铁离子可以选用K3[Fe(CN)6]溶液或盐酸酸化的BaCl2故答案为:bd;
,为验证二氧化硫的还原性,可以检验E中的溶液中是否有Fe2+或SO42-生成。NH4SCN溶液不能检验这两种离子;亚铁离子能与K3[Fe(CN)6]溶液生成蓝色沉淀;Cl-也有还原性,故不能用酸性KMnO4溶液检验Fe2+;盐酸酸化的BaCl2溶液可以检验SO42-,则检验反应生成的亚铁离子可以选用K3[Fe(CN)6]溶液或盐酸酸化的BaCl2故答案为:bd;![]() ;
;
(6)Cu2O和Cu为红色固体,根据题意Cu2O和硫酸反应生成Cu2+和Cu,而Cu不和稀硫酸反应,Cu2O和Cu都能与硝酸反应生成硝酸铜蓝色溶液,则验证固体产物中是否有Cu2O,可用Cu2+的颜色来区别,若溶液变为蓝色证明有Cu2O存在;硝酸可以溶解Cu及其氧化物得到蓝色溶液,不可行;氢气可以把氧化亚铜还原为同样是红色的Cu,不可行。故选乙,故答案为:乙;
(7)由元素化合价的变化可知,Cu2O和SO2是还原产物,O2是氧化产物,设O2为xmol,Cu2O为ymol,由题意可知SO2为![]() mol,由得失电子数目守恒可得4x=2y+
mol,由得失电子数目守恒可得4x=2y+![]() ×2,解得x=
×2,解得x=![]() ,由CuO、Cu2O的质量之比为5:9可知物质的量比为
,由CuO、Cu2O的质量之比为5:9可知物质的量比为![]() :
:![]() =1:1,因SO2、O2、SO3的体积之比(同温同压下测定)为4:3:2,则CuO、Cu2O、SO3、SO2和O2的物质的量之比为y:y:
=1:1,因SO2、O2、SO3的体积之比(同温同压下测定)为4:3:2,则CuO、Cu2O、SO3、SO2和O2的物质的量之比为y:y:![]() :x:
:x:![]() = y:y:y:
= y:y:y:![]() :2y=2:2:2:3:4,则反应的化学方程式为
:2y=2:2:2:3:4,则反应的化学方程式为![]() ,故答案为:
,故答案为:![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】400℃时,向一个容积为2L的密闭容器中充入一定量的CO和H2,发生如下反应:CO(g)+2H2(g)![]() CH3OH(g)。反应过程中测得的部分数据见下表:
CH3OH(g)。反应过程中测得的部分数据见下表:
t/min | 0 | 10 | 20 | 30 |
n(CO)/mol | 0.20 | 0.08 | 0.04 | |
n(H2)/mol | 0.40 | 0.08 |
下列说法不正确的是
A. 反应在前10min内的平均速率为v(H2)=0.012 mol/(L·min)
B. 400℃时,该反应的平衡常数数值为2.5×103
C. 保持其他条件不变,升高温度,平衡时c(CH3OH)=0.06mol·L-1,则反应的ΔH<0
D. 相同温度下,若起始时向容器中充入0.3mol CH3OH,达到平衡时CH3OH的转化率大于20%
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A.AB.BC.CD.D
【题目】半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g)。半水煤气经过下列步骤转化为合成氨的原料。
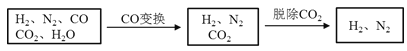
完成下列填空:
(1)半水煤气含有少量硫化氢。将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证明有硫化氢存在。
(2)半水煤气在铜催化下实现CO变换:CO+H2O![]() CO2+H2
CO2+H2
若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)=____________。
(3)碱液吸收法是脱除二氧化碳的方法之一。已知:
Na2CO3 | K2CO3 | |
20℃碱液最高浓度(mol/L) | 2.0 | 8.0 |
碱的价格(元/kg) | 1.25 | 9.80 |
若选择Na2CO3碱液作吸收液,其优点是__________;缺点是____________。如果选择K2CO3碱液作吸收液,用什么方法可以降低成本?
___________________________________________
写出这种方法涉及的化学反应方程式。_______________________
(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案。
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数。
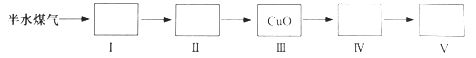
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
②该实验方案中,步骤Ⅰ、Ⅱ的目的是:_________________。
③该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数。