题目内容
【题目】下列关于图像的描述错误的是( )
A.图I表示向盐酸中滴加NaAlO2溶液,沉淀质量随NaAlO2溶液体积的变化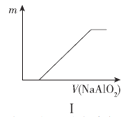
B.图II表示向NH4Al(SO4)2溶液中滴加NaOH溶液,沉淀质量随NaOH溶液体积的变化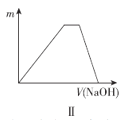
C.图III表示向NH4Cl溶液中加入稍过量Na2O2固体,产生气体的体积随Na2O2质量的变化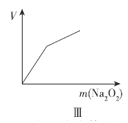
D.图IV表示向Na2CO3溶液中滴加稀盐酸,产生气体的体积随盐酸溶液体积的变化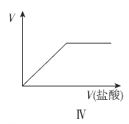
【答案】D
【解析】
A.向盐酸中滴加NaAlO2溶液,先生成AlCl3,开始一段时间内没有沉淀生成,当盐酸全部转化为AlCl3后,AlCl3与NaAlO2反应生成氢氧化铝沉淀,图象符合,故A正确;
B.向NH4Al(SO4)2溶液中滴加NaOH溶液,氢氧化钠先与铝离子反应生成氢氧化铝沉淀,然后氢氧化钠与铵根离子反应,最后氢氧化钠与氢氧化铝反应,沉淀完全溶解,图象符合,故B正确;
C.向NH4Cl溶液中加入稍过量Na2O2固体,开始一段时间内,生成氧气和氨气,气体体积增大的较快,当过氧化钠过量时,只是过氧化钠与水反应,只有氧气生成,气体的体积增大的较慢,图象符合,故C正确;
D.Na2CO3溶液中滴加稀盐酸,开始生成碳酸氢钠和NaCl,所以开始一段时间内没有气体生成,当碳酸钠全部转化为碳酸氢钠,碳酸氢钠与盐酸反应生成气体,所以一开始时没有气体生成,图象不符合,故D错误;
答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】现有X、Y、Z、T四种短周期元素,原子序数依次增大。请根据下列相关信息,回答问题。
元素 | 相关信息 |
X | 原子的1s轨道上只有1个电子 |
Y | 原子的L层上s电子数等于p电子数 |
Z | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的 |
T | 负二价的元素T的氢化物在通常情况下是一种液体,且T的质量分数为88.9% |
(1) Z2X4分子中Z原子采取________杂化,写出与之互为等电子体的有机物的结构简式_____________________
(2) Cl2T分子的空间构型___________, Z2T的电子式_________________
(3) 请用价层电子对互斥理论解释ZX![]() 和ZX3的键角∠XZX的大小:_____________。
和ZX3的键角∠XZX的大小:_____________。
(4) Y晶体的晶胞如图所示,该晶胞含有______个Y原子,若晶胞的密度为d g·cm-3,阿伏加德罗常数的值为NA(mol-1),则晶胞参数为a=_______ pm。(用含d 、NA的式子表示)
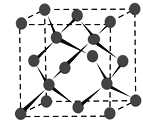
【题目】四种短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Z元素的最外层电子数是内层电子总数的![]() 。下列说法不正确的是
。下列说法不正确的是
X | Y | |
Z | W |
A.Z元素位于周期表的第3周期第VA族
B.X、W元素的最高价氧化物对应水化物的酸性:W强于X
C.Y元素的气态氢化物的热稳定性比Z的高
D.X和Y都只能形成一种氧化物
【题目】实验小组同学对乙醛与新制的Cu(OH)2反应的实验进行探究。
实验Ⅰ:取2mL 10%的氢氧化钠溶液于试管中,加入5滴2%的CuSO4溶液和5滴5%的乙醛溶液,加热时蓝色悬浊液变黑,静置后未发现红色沉淀。
实验小组对影响实验Ⅰ成败的因素进行探究:
(1)探究乙醛溶液浓度对该反应的影响。
编号 | 实验Ⅱ | 实验Ⅲ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变红棕色,静置后底部有大量红色沉淀 | 加热,蓝色悬浊液变红棕色,静置后上层为棕黄色油状液体,底部有少量红色沉淀 |
已知:乙醛在碱性条件下发生缩合反应:CH3CHO+CH3CHO![]() CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
① 能证明乙醛被新制的Cu(OH)2 氧化的实验现象是______。
② 乙醛与新制的Cu(OH)2 发生反应的化学方程式是______。
③ 分析实验Ⅲ产生的红色沉淀少于实验Ⅱ的可能原因:______。
(2)探究NaOH溶液浓度对该反应的影响。
编号 | 实验Ⅳ | 实验Ⅴ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,蓝色悬浊液变红棕色, 静置后底部有红色沉淀 |
依据实验Ⅰ→Ⅴ,得出如下结论:
ⅰ. NaOH溶液浓度一定时,适当增大乙醛溶液浓度有利于生成Cu2O。
ⅱ. 乙醛溶液浓度一定时,______。
(3)探究NaOH溶液浓度与乙醛溶液浓度对该反应影响程度的差异。
编号 | 实验Ⅵ | 实验Ⅶ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,静置后底部有红色沉淀 |
由以上实验得出推论: ______。