题目内容
(12分)某可逆反应从0—2分钟进行过程中, 在不同反应时 间各物质的量的变化情况如下图所示。则该反应的的反应物是 ,生成物是 ,化学方程式为 ;反应开始至2分钟时,能否用C表示反应速率?若能,其反应速率为 _____ ,若不能,则其原因为 _ ________________ ;2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了 ____ 状态。
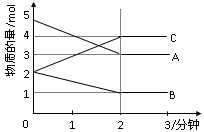

A和B;C;2A+B 2C;不能;无体积,无法求出浓度变化值;化学平衡
2C;不能;无体积,无法求出浓度变化值;化学平衡
 2C;不能;无体积,无法求出浓度变化值;化学平衡
2C;不能;无体积,无法求出浓度变化值;化学平衡试题分析:根据图示可知:在反应中A、B减少,C增加。所以A、B是反应物,C是生成物。它们反应时的物质的量的比为2:1:2,最终达到平衡。所以化学反应方程式是2A+B
 2C;反应开始至2分钟时,由于只知道物质的量的变化,而不知道容器的容积,所以不能否用C表示反应速率。2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了平衡状态。
2C;反应开始至2分钟时,由于只知道物质的量的变化,而不知道容器的容积,所以不能否用C表示反应速率。2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了平衡状态。
练习册系列答案
相关题目
下列措施对增大化学反应速率明显有效的是
| A.Na与水反应时增大水的用量 |
| B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| C.在K2SO4与BaCl2两溶液反应时,增大压强 |
| D.将铝片改为铝粉,做铝与氧气反应的实验 |
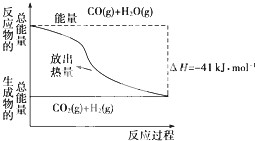
 Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
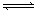 XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法: