题目内容
(4分)在一固定容积的密闭容器中,a mol/LN2和b mol/L H2反应,一定条件下经过2min达到平衡,生成c mol/L NH3.
求:(1)用H2表示的速率是多少?(2)N2的转化率是多少?
求:(1)用H2表示的速率是多少?(2)N2的转化率是多少?
(1)3c/4 mol/(L.min) (2)c/2a×100﹪
试题分析:(1)发生反应的方程式是:N2+3H2
 2NH3。一定条件下经过2min达到平衡,生成c mol/L NH3.根据反应方程式中氢气与氨气的关系可知反应消耗的氢气的浓度是3/2c,则V(H2)="ΔC÷Δt=" 3/2c mol/L÷2min="3c/4" mol/(L.min);(2)根据反应方程式可知:每消耗1mol的N2,反应产生2mol的氨气,现在c mol/L NH3,则消耗氮气的浓度是c/2mol/L,所以氮气的转化率是c/2mol/L÷amol/L×100﹪= c/2a×100﹪.
2NH3。一定条件下经过2min达到平衡,生成c mol/L NH3.根据反应方程式中氢气与氨气的关系可知反应消耗的氢气的浓度是3/2c,则V(H2)="ΔC÷Δt=" 3/2c mol/L÷2min="3c/4" mol/(L.min);(2)根据反应方程式可知:每消耗1mol的N2,反应产生2mol的氨气,现在c mol/L NH3,则消耗氮气的浓度是c/2mol/L,所以氮气的转化率是c/2mol/L÷amol/L×100﹪= c/2a×100﹪.
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


 2Z(g)
2Z(g)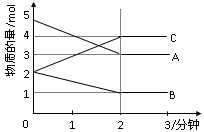
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
 C(s)+H20(g) △H>O化学反应速率(V)与时间(t)的关系,图二表示的是可逆反应2N02(g)
C(s)+H20(g) △H>O化学反应速率(V)与时间(t)的关系,图二表示的是可逆反应2N02(g) 
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)