题目内容
18.标准状况下,气态分子断开1mol化学键所需的能量称为键能.已知H-H,H-O,和O═O键的键能分别为436KJ/mol,463KJ/mol,495KJ/mol,下列热化学方程式正确的是( )| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=-485KJ/mol | B. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+485KJ/mol | ||
| C. | 2 H2(g)+O2(g)═2 H2O(g)△H=+485KJ/mol | D. | 2 H2(g)+O2(g)═2 H2O(g)△H=-485KJ/mol |
分析 旧键断裂需要吸收能量,新键的生成会放出能量,△H=反应物的键能和-生成物的键能和,据此进行解答.
解答 解:A、水分解是吸热反应,应该△H>0,故A错误;
B、水分解是吸热反应,H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=2×463kJ/mol-436kJ/mol-$\frac{1}{2}$×495kJ/mol=242.5kJ/mol,故B错误;
C、氢气燃烧放热,应该△H<0,故C错误;
D、氢气燃烧放热,2H2(g)+O2(g)═2 H2O(g)△H=2×436kJ/mol+495kJ/mol-4×463kJ/mol=-485kJ/mol,故D正确.
故选:D.
点评 本题考查了热化学方程式的书写、反应热的计算,题目难度中等,注意掌握热化学方程式的书写原则,明确化学键与化学反应中能量变化的关系是解题关键.

练习册系列答案
相关题目
4.BaSO4饱和溶液中加少量的BaCl2溶液产生BaSO4沉淀,若以Ksp表示BaSO4的溶度积常数,则平衡后溶液中( )
| A. | c (Ba2+)=c(SO42-)=(Ksp)${\;}^{\frac{1}{2}}$ | B. | c(Ba2+)•c(SO42-)>Ksp,c(Ba2+)=c(SO42-) | ||
| C. | c(Ba2+)•c(SO42-)=Ksp,c(Ba2+)>c(SO42-) | D. | c(Ba2+)•c(SO42-)≠Ksp,c(Ba2+)<c(SO42-) |
13.ClCH=CH-CH3能发生的反应有( )
①加聚 ②与硝酸银溶液生成白色沉淀 ③使溴水褪色 ④消去 ⑤加成 ⑥取代.
①加聚 ②与硝酸银溶液生成白色沉淀 ③使溴水褪色 ④消去 ⑤加成 ⑥取代.
| A. | 都可以 | B. | 只有①不能发生 | C. | 只有②不能发生 | D. | 只有①④不能发生 |
3.下列关于糖类、蛋白质、油脂的说法中,正确的是( )
| A. | 氨基酸、多肽、蛋白质都具有两性 | |
| B. | 利用油脂在酸性条件下水解,可以产生甘油和肥皂 | |
| C. | 淀粉与纤维素分子式都为(C6H10O5)n,但结构不同,所以它们互为同分异构体 | |
| D. | 饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析 |
10.将物质的量浓度之比为1:2的X(g)与Y(g)在密闭容器中进行反应:X(g)+2Y(g)=3Z(g)+Q(s)△H>O,下列叙述一定正确的是( )
| A. | 当容器中X与Y的物质的量浓度之比满足1:2时,反应达到平衡 | |
| B. | 达到平衡后,反应速率3v正(Y)=2v逆(z) | |
| C. | 达到平衡时,X的转化率为25%,则平衡常数K值为$\frac{1}{16}$ | |
| D. | 达到平衡后,升高温度,X的体积分数增大 |
8.元素周期表中有相邻元素A、B、C,A与B同周期,B与C同主族,它们的原子最外层电子数之和为19,原子序数之和为33,则( )
| A. | B位于第二周期第ⅣA族 | |
| B. | A在同周期元素中原子半径最小 | |
| C. | A、B没有最高正化合价 | |
| D. | B、C所形成的化合物会引发温室效应 |
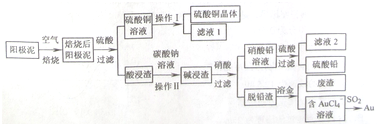
 利用如图装置可验证酸的强弱规律.
利用如图装置可验证酸的强弱规律.