题目内容
2.下列关于各实验装置图的叙述中正确的是( )| A. | 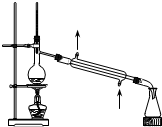 装置可用于分离苯和溴苯的混合物 | B. | 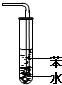 装置可用于吸收HCl或NH3气体 | ||
| C. |  用图所示装置分离乙醇与乙酸 | D. | 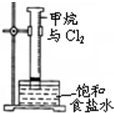 图中量筒中发生了加成反应 |
分析 A.分离互溶的液体应该采用蒸馏方法;
B.有缓冲作用的装置能防倒吸;
C.互不相溶的液体应该采用分液方法分离;
D.光照条件下,氯气和甲烷发生取代反应.
解答 解:A.分离互溶的液体应该采用蒸馏方法,苯和溴苯互溶,应该利用其沸点不同采用蒸馏方法分离,故A正确;
B.有缓冲作用的装置能防倒吸,氯化氢和氨气极易溶于水,该装置没有缓冲作用,不能防止倒吸,应该用四氯化碳和水混合,故B错误;
C.互不相溶的液体应该采用分液方法分离,乙醇和乙酸互溶而不能采用分液方法分离,应该采用蒸馏方法分离,故C错误;
D.光照条件下,氯气和甲烷发生取代反应而不是加成反应,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及尾气处理、物质分离和提纯、反应类型判断等知识点,明确物质性质及实验原理即可解答,会根据物质不同性质选取合适的分离方法,题目难度不大.

练习册系列答案
相关题目
12.下列根据实验现象所作出的结论中正确的是( )
| A. | 某盐溶液中加入NaOH溶液有白色沉淀出现,则原溶液中一定含有Mg2+ | |
| B. | 某溶液中加入AgNO3溶液有白色沉淀出现,则原溶液中一定含有Cl- | |
| C. | 某溶液中加入盐酸产生能使澄清石灰水变浑浊的无色无味的气体,则原溶液中一定含有${CO}_{3}^{2-}$和${HCO}_{3}^{-}$中的一种 | |
| D. | 某盐溶液中加入NaOH溶液并加热,能产生使湿润的蓝色石蕊试纸变红的气体,则原溶液中一定含有${NH}_{4}^{+}$ |
13.卤族元素随着原子序数的增大,下列递变规律正确的是( )
| A. | 单质熔、沸点逐渐降低 | B. | 单质的氧化性逐渐增强 | ||
| C. | 气态氢化物沸点逐渐升高 | D. | 气态氢化物稳定性逐渐减弱 |
17.下列关于有机物的描述正确的是( )
| A. | 葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 | |
| B. | 淀粉、油脂和蛋白质都能发生水解反应,淀粉水解的最终产物可与新制的Cu(OH)2反应 | |
| C. | 多糖、蛋白质、脂肪和聚丙烯都属于高分子化合物 | |
| D. | 汽油、柴油、植物油、棉、麻、丝、毛完全燃烧只生成CO2和H2O |
7.某二元酸(H2A)在水中的电离方程式为H2A═H++HA-,HA-?H++A2-(25℃时,Ka=1.0×10-2),下列有关说法中正确的是( )
| A. | H2A是弱酸 | |
| B. | 稀释0.1mol/L H2A溶液,因电离平衡向右移动而导致c(H+)增大 | |
| C. | 在0.1mol/L的H2A溶液中,c(H+)=0.12mol/L | |
| D. | 若0.1mol/L的NaHA溶液中c(H+)=0.02mol/L,则0.1mol/L的H2A溶液中c(H+)<0.12mol/L |
6.下列有关物质性质或应用的说法正确的是( )
| A. | 二氧化锰具有强氧化性,能将双氧水氧化为氧气 | |
| B. | Zn具有氧化性和导电性,可用作锌锰干电池的负极材料 | |
| C. | 炭具有强还原性,高温下能将二氧化硅还原为硅 | |
| D. | 二氧化硫具有漂白性,与氯水混合使用效果会更好 |
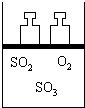 如图所示,将4mol SO2和2mol O2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态A时,测得气体总物质的量为4.2mol.若SO2、O2、SO3的起始物质的量分别用a、b、c 表示,试回答:
如图所示,将4mol SO2和2mol O2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态A时,测得气体总物质的量为4.2mol.若SO2、O2、SO3的起始物质的量分别用a、b、c 表示,试回答: