��Ŀ����
����Ŀ������أ�KIO3������Ҫ��ʳƷ���Ӽ���ij��ѧ��ȤС��������в�����ȡKIO3�������в�Ʒ�Ĵ��Ȳⶨ��
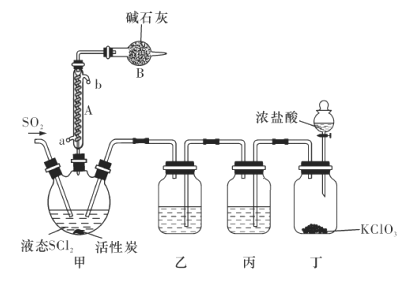
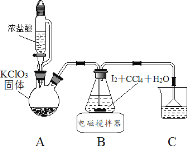
��ȡ���ᣨHIO3����ʵ��װ��ʾ��ͼ���й��������£�
HIO3 | �ٰ�ɫ���壬������ˮ�����������Ȼ�̼ ��Ka��0.169mol��L��1 |
KIO3 | �ٰ�ɫ���壬������ˮ���������Ҵ� �ڼ���������������Ӧ�� ClO��+ IO3- ��IO4 -+ Cl- |
�ش��������⣺
������� Cl2 ���� I2 ��ȡ HIO3
��1��װ�� A �з�����Ӧ�Ļ�ѧ����ʽ_______��
��2��װ�� B �е� CCl4 ���Լӿ췴Ӧ���ʣ�ԭ��_______��
��3����Ӧ������ȡ HIO3 ��Һ�IJ����У����貣���������ձ���________��_______��
������� KOH �к� HIO3 ��ȡ KIO3
��4�����кͷ�Ӧ�����ӷ���ʽΪ_______���к�֮ǰ��Ӧ������ HIO3��Һ������ӽ���ɫ�������к�ʱ������_______���ѧʽ�������� KIO3 �IJ�����
��5�����кͺ����Һ�м�������_______�������衢���á����˵Ȳ������õ���ɫ���塣
��6��Ϊ��֤���ȡ����������������ˮ���μ����� SO2 ������Һ��ҡ�ȣ��ټ��뼸�ε�����Һ����Һ��������ʵ��ʱ�����ӵ� SO2 ������Һ������������ɫ���֣�ԭ����_______��
����Ȳⶨ
��7��ȡ 0.1000 g ��Ʒ�ڵ���ƿ�У�����ϡ��������� KI ��Һ���� 0.1000 mol��L��1Na2S2O3��Һ�ζ����ӽ��յ�ʱ���������ָʾ���������ζ����յ㣬��ɫ��ʧ��I2+2S2O32-��2I-+S4O62-��������ƽ��ʵ���ƽ������ Na2S2O3 ��Һ�����Ϊ 24.00 mL�����Ʒ�� KIO3 ����������Ϊ_______��[M��KIO3����214.0 g��mol-1]
���𰸡�KClO3+6HCl(Ũ)=KCl+3Cl2��+3H2O I2��Cl2������CCl4�������˷�Ӧ��Ũ�� ��Һ©�� ������ HIO3+OH=IO3+H2O ClO �Ҵ�(�����ƾ�����C2H5OH��) ������SO2�ܽ�IO3-��I2�Ȼ�ԭΪI 85.60%
��������
��������Cl2����I2��ȡHIO3��Aװ���Ʊ�������Bװ��Cl2����I2��ȡHIO3��Cװ������β������������KOH�к�HIO3��ȡKIO3��1����ʵ��ԭ����װ��ͼ��֪��װ��A������غ�Ũ������ȡ������ͬʱ����KCl��ˮ���ݴ���д����2������Cl2��I2��ˮ���ܽ��С����CCl4���ܽ��ȴ�ܴ�������Ӧ��Ũ�ȣ��ݴ˿ɵã���3������������Ϣ��֪��B�з�Ӧ������ĵ�����Ҫ��ˮ��Һ������CCl4�������ܣ����Ա�����÷�Һ���Ի�ȡ������Һ��
��4��KOH��HIO3�����кͷ�Ӧ����KIO3��ˮ���ݴ���д���к�֮ǰ��Һ�д��ڽ϶�Cl2���к�ʱCl2ת��ΪClO-��������֪������������������Ӧ��ClO-+IO3-=IO4-+Cl-����������5������KIO3�������Ҵ���������6��SO2���л�ԭ�ԣ�������SO2��IO3-��I2�Ȼ�ԭΪI-����7��ȡ0.1000 g��Ʒ�ڵ���ƿ�У�����ϡ���������KI��Һ��������Ӧ��IO3-+5I-+6H+=3I2+3H2O����0.1000 molL-1Na2S2O3��Һ�ζ����ɵ�I2������KIO3��3I2��6S2O32-��ϵʽ���ɼ�������
��1��װ��A������ȡ��������ӦΪ��KClO3+6HCl(Ũ)=KCl+3Cl2��+3H2O���ʴ�Ϊ��KClO3+6HCl(Ũ)=KCl+3Cl2��+3H2O��
��2������Cl2��I2��ˮ���ܽ��С����CCl4���ܽ��ȴ�ܴ�װ��B�е�CCl4������Ӧ��Ũ�ȣ�ʹ��Ӧ���ʼӿ죬�ʴ�Ϊ��I2��Cl2������CCl4�������˷�Ӧ��Ũ�ȣ�
��3������������Ϣ��֪��B�з�Ӧ������ĵ�����Ҫ��ˮ��Һ������CCl4�������ܣ����Ա�����÷�Һ���Ի�ȡ������Һ����Һ��Ҫ�IJ����������ձ�����Һ©�������������ʴ�Ϊ����Һ©������������
��4��KOH��HIO3�����кͷ�Ӧ����KIO3��ˮ��HIO3����������ʣ������ӷ���ʽ�б�����ѧʽ�������ӷ���ʽΪ��HIO3+OH=IO3+H2O���к�֮ǰ��Һ�д��ڽ϶�Cl2��ͨ��������п��Գ�ȥCl2�������к�ʱCl2ת��ΪClO��ClO-��һ����IO3����ΪIO4���Ӷ�����KIO3�����½����ʴ�Ϊ��HIO3+OH=IO3+H2O��ClO��
��5��KIO3�������Ҵ������������Ҵ�����ʹKIO3����Һ�������������кͺ����Һ�м��������Ҵ��������衢���á����˵Ȳ������õ���ɫ���壻�ʴ�Ϊ���Ҵ�(�����ƾ�����C2H5OH��)��
��6���������֪����������SO2ˮ��Һ�ܽ�KIO3��ԭΪI2���������������SO2ˮ��Һȴ����ɫ���֣�˵��������SO2�ܽ�IO3-��I2�Ȼ�ԭΪI���ʴ�Ϊ��������SO2�ܽ�IO3-��I2�Ȼ�ԭΪI��
��7��ȡ0.1000g��Ʒ�ڵ���ƿ�У�����ϡ���������KI��Һ��������Ӧ��IO3+5I+6H+=3I2+3H2O����0.1000 mol/LNa2S2O3��Һ�ζ����ɵ�I2���й�ϵʽ��KIO33I26S2O32����n(KIO3)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() ��0.1000mol/L��0.024L=0.0004mol�� �ʲ�Ʒ��KIO3����������Ϊ
��0.1000mol/L��0.024L=0.0004mol�� �ʲ�Ʒ��KIO3����������Ϊ![]() ��100%=85.60%���ʴ�Ϊ��85.60%��
��100%=85.60%���ʴ�Ϊ��85.60%��

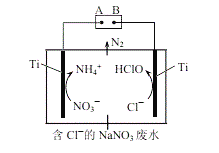
����Ŀ��������һ�ֳ��õĻ�ԭ����ijУ������ѧС��̽�����ᱻ�������������⡣
ʵ��� | �Լ� | ��Ϻ� ��ҺpH | ���� ��1h����Һ�� | ||
�Թ� | �ι� | ||||
| a | 4mL0.01mol��L1 KMnO4��Һ������ŨH2SO4 | 2mL0.3mol��L1H2C2O4 ��Һ | 2 | ��Ϊ��ɫ |
b | 4mL0.01mol��L1KMnO4��Һ������ŨNaOH | 7 | �����Ա仯 | ||
c | 4mL0.01mol��L1 K2Cr2O7��Һ������ŨH2SO4 | 2 | �����Ա仯 | ||
d | 4mL0.01mol��L1 K2Cr2O7��Һ������ŨNaOH | 7 | �����Ա仯 | ||
��1��H2C2O4�Ƕ�Ԫ���ᣬд��H2C2O4����ˮ�ĵ��뷽��ʽ��_____________��
��2��ʵ��I�Թ�a��KMnO4���ձ���ԭΪMn2+���÷�Ӧ�����ӷ���ʽΪ��________��
��3�������ͳ����������ϣ�ʵ��I�Թ�c��H2C2O4��K2Cr2O7��Һ��Ӧ������ʱ�������ɣ�������MnO2�ɴٽ�H2C2O4��K2Cr2O7�ķ�Ӧ�����ݴ����ϣ����������������ʵ��֤ʵ����һ�㡣
ʵ�� | ʵ��III | ʵ��IV | |
ʵ����� |
|
|
|
ʵ������ | 6 min�������ȫ�ܽ⣬��Һ��ɫ��dz���¶Ȳ��� | 6 min�����δ�ܽ⣬��Һ��ɫ�����Ա仯 | 6 min�����δ�ܽ⣬��Һ��ɫ�����Ա仯 |
ʵ��IV��Ŀ���ǣ�_______________________��
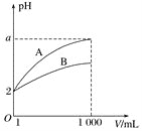
��4�������ȶ�ʵ��II��������̽����������Һ��Cr2O72- Ũ�ȱ仯��ͼ��

�갺Ͳ̲���Ϊ�˱仯��ͨ����������ʵ�ֵġ�
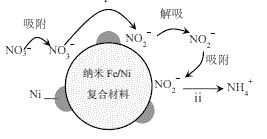
����i��MnO2��H2C2O4��Ӧ������Mn2+��
����ii��__________________________________��
�ٲ������ϣ���Һ��Mn2+�ܱ�PbO2����ΪMnO4-����Թ���i���ɲ������·���֤ʵ����0.0001molMnO2���뵽6mL____________�У�������ȫ�ܽ⣻����ȡ��������Һ���������PbO2���壬��ַ�Ӧ���ã��۲쵽_______________��
�ڲ����������ʵ�鷽��֤ʵ�˹���ii���������ǵ�ʵ�鷽����________��
��5���ۺ�����ʵ���֪�����ᷢ��������Ӧ��������__________________�йء�