题目内容
【题目】锌空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,放电时反应为:2Zn+O2+4OH-+2H2O=2![]() 。下列说法正确的是
。下列说法正确的是
A.放电时,正极反应为:Zn+4OH--2e-=![]()
B.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
C.充电时,电解质溶液中c(OH-)逐渐增大
D.充电时,电子的运动方向为:电源负极→电解池阴极→电解质溶液→电解池阳极→电源正极
【答案】C
【解析】
根据2Zn+O2+4OH-+2H2O═2![]() 可知,O2中元素的化合价降低,被还原,应为原电池正极,电极反应式为:O2+2H2O+4e-=4OH-;Zn元素化合价升高,被氧化,应为原电池负极,电极反应式为Zn+4OH--2e-═
可知,O2中元素的化合价降低,被还原,应为原电池正极,电极反应式为:O2+2H2O+4e-=4OH-;Zn元素化合价升高,被氧化,应为原电池负极,电极反应式为Zn+4OH--2e-═![]() ,充电时阳离子向阴极移动,以此解答该题。
,充电时阳离子向阴极移动,以此解答该题。
A.根据分析,放电时,负极反应式为:Zn+4OH--2e-=![]() ,故A错误;
,故A错误;
B.放电时,正极的电极反应式为:O2+2H2O+4e-=4OH-,每消耗标况下22.4L氧气,转移电子4mol,所以电路中通过2mol电子,消耗氧气11.2L(标准状况),故B错误;
C.充电时为电解池,电解反应为2![]()
![]() 2Zn+O2+4OH-+2H2O,电解质溶液中c(OH-)逐渐增大,故C正确;
2Zn+O2+4OH-+2H2O,电解质溶液中c(OH-)逐渐增大,故C正确;
D.充电时为电解池,电子经外电路由电解池阳极→电源正极→电源负极→电解池阴极,电子不能再溶液中传递,故D错误;
答案选C。

【题目】初始温度为t ℃,向三个密闭的容器中按不同方式投入反应物,发生如下反应:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1,测得反应的相关数据如下:
2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1,测得反应的相关数据如下:
容器 | 容器类型 | 初始体积 | 初始压强/Pa | 反应物投入量/mol | 平衡时Cl2的物质的量/mol | |||
HCl | O2 | Cl2 | H2O | |||||
I | 恒温恒容 | 1L |
| 4 | 1 | 0 | 0 | 1 |
II | 绝热恒容 | 1L | p2 | 0 | 0 | 2 | 2 | a |
III | 恒温恒压 | 2L | p3 | 8 | 2 | 0 | 0 | b |
下列说法正确的是( )
A.反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
B.a>1, b>2
C.p2=1.6×105Pa,p3=4×105Pa
D.若起始向容器Ⅰ中充入0.5 mol HCl、0.5 mol O2、0.5 mol Cl2和0.5 mol H2O,则反应向逆反应方向进行
【题目】镧系为元素周期表中第ⅢB族、原子序数为5771的元素。
(1)镝Dy)的基态原子电子排布式为[Xe] 4f106s2,画出镝(Dy)原子价层电子排布图:____________.
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为____________。
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是_____填元素名称)。
几种镧系元素的电离能(单位:kJmol-1)
元素 | Ⅰ1 | Ⅰ2 | Ⅰ3 | Ⅰ4 |
Yb (镱) | 604 | 1217 | 4494 | 5014 |
Lu (镥) | 532 | 1390 | 4111 | 4987 |
La (镧) | 538 | 1067 | 1850 | 5419 |
Ce (铈) | 527 | 1047 | 1949 | 3547 |
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为_______(用元素符号表示)。
②画出氨的最简单气态氢化物水溶液中存在的氢键:________(任写一种)。
③元素Al也有类似成键情况,气态氯化铝分子表示为((AlCl3)2,分子中A1原子杂化方式为_____,分子中所含化学键类型有 _______(填字母)。
a.离子键 b.极性键 c.非极性键 d.配位键
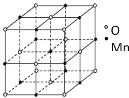
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中错原子位于面心和顶点,则PrO2 (二氧化镨)的晶胞中有_____个氧原子;已知晶胞参数为apm,密度为ρgcm-3,NA=_______(用含a、ρ的代数式表示)。