题目内容
【题目】H是一种重要的化工原料,它可由石油和煤焦油通过下列路线合成:
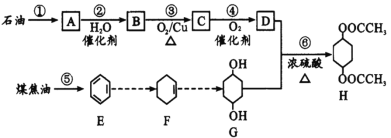
(1)A的名称是____;过程①是____变化(填“物理”或“化学”,下同),过程⑤是_______变化。
(2)反应③的化学方程式为_______;反应⑥的类型为_________。
(3)鉴别E与F的方法是_________________。
(4)H中六元环上的氢原子被两个氯原子取代后的有机物有___种。
【答案】乙烯 化学 物理 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 取代反应或酯化反应 分别滴入酸性 KMnO4 溶液, 振荡,使 KMnO4 溶液褪色的是 F,不褪色的是 E 7
2CH3CHO+2H2O 取代反应或酯化反应 分别滴入酸性 KMnO4 溶液, 振荡,使 KMnO4 溶液褪色的是 F,不褪色的是 E 7
【解析】
由H的结构及反应条件可以推断D为乙酸,则结合各步变化的反应条件可以推断C为乙醛、B为乙醇、A为乙烯。
(1)A的名称是乙烯;工业上通常对石油分馏产品进行裂解来获得乙烯,故过程①为裂解,是化学变化;工业上通过对煤焦油进行分馏而获得苯,过程⑤为分馏,是物理变化。
(2)反应③为乙醇的催化氧化,化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;反应⑥为乙酸与环己二醇反应生成酯,故为酯化反应或取代反应。
2CH3CHO+2H2O;反应⑥为乙酸与环己二醇反应生成酯,故为酯化反应或取代反应。
(3)E分子中没有碳碳双键,而F分子中有碳碳双键,因此,鉴别E与F的方法是:分别滴入酸性 KMnO4 溶液,振荡,使 KMnO4 溶液褪色的是 F,不褪色的是 E。
(4)用定一议二法,H分子有一定的对称性,六元环上的6个碳原子均有H原子可以被取代,如图所示 ,可以先把1号或2号的H原子取代,然后分析另一个H原子被取代的可能性,先取代1,环上其他碳原子上的H均可以被取代,但要注意左右对称,故有3种;再先取代2,则与1相同的位置不能再取代,可以找到4种,注意2号碳上有2个H原子可以被取代。综上所述,可以确定H中六元环上的氢原子被两个氯原子取代后的有机物有7种。
,可以先把1号或2号的H原子取代,然后分析另一个H原子被取代的可能性,先取代1,环上其他碳原子上的H均可以被取代,但要注意左右对称,故有3种;再先取代2,则与1相同的位置不能再取代,可以找到4种,注意2号碳上有2个H原子可以被取代。综上所述,可以确定H中六元环上的氢原子被两个氯原子取代后的有机物有7种。

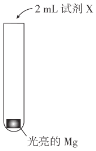
【题目】实验小组研究Mg与NH4Cl溶液的反应,实验如下:
| 实验 | 试剂X | 现象 |
Ⅰ | H2O | 产生极少气泡,Mg表面逐渐变暗,反应很快停止 | |
Ⅱ | 1mol/LNH4Cl溶液(pH=5) | 数分钟内持续产生较多气泡(经检验含有H2),溶液中出现大量白色固体,试管变热 |
(1)Ⅰ中Mg表面变暗,说明产生了Mg(OH)2固体。反应很快停止的原因是__。
(2)探究实验Ⅰ、Ⅱ产生气泡差异的原因。
假设一:NH4Cl溶液显酸性,c(H+)较大,与Mg反应速率较快。
①用离子方程式表示NH4Cl溶液显酸性的原因:___。
测定实验Ⅱ反应过程中溶液pH随时间的变化,结果如下:

②假设一__(填“是”或“不是”)实验Ⅰ、Ⅱ产生气泡差异的主要原因。
假设二:NH4Cl溶液中的NH![]() 溶解Mg(OH)2固体,使Mg能够持续与水反应。
溶解Mg(OH)2固体,使Mg能够持续与水反应。
进行实验:向1mol/LNH4Cl溶液中加几滴氨水,使溶液pH≈8,得到溶液a。向少量Mg(OH)2固体中加入2mL溶液a,固体溶解。
③有同学认为假设二的实验不严谨,需增加对比实验:__(填操作和现象),说明假设二正确。
④向NH4Cl溶液中加几滴氨水的目的是___。
(3)1min后,实验Ⅱ中还检测到少量NH3。
①检测NH3时要使用湿润的___试纸。
②气体中含有少量NH3的原因是__。
(4)Mg与NH4Cl溶液充分反应后,仍有大量Mg(OH)2固体生成。综合上述实验,解释Mg与NH4Cl溶液的反应比Mg与H2O的反应更剧烈的主要原因:__。
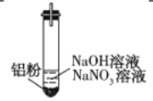
【题目】某无色溶液中可能含有H+、OH-、Na+、K+、NO![]() ,加入铝粉后,只产生H2,为探究该溶液中存在的离子,某学习小组进行了如下实验。
,加入铝粉后,只产生H2,为探究该溶液中存在的离子,某学习小组进行了如下实验。
(1)甲同学分析“若H+大量存在,则NO![]() 就不能大量存在”,设计实验证实如下:
就不能大量存在”,设计实验证实如下:
装置 | 现象 |
| Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,液面上方出现浅棕色气体 Ⅲ.试管变热,溶液沸腾 |
①现象Ⅲ产生的原因___。
②根据现象Ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
实验 | 内容 | 现象 |
实验1 | 将湿润KI—淀粉试纸置于空气中 | 试纸未变蓝 |
实验2 | 用湿润KI—淀粉试纸检验浅棕色气体 | 试纸变蓝 |
实验1、2说明反应生成了NO。
请用化学方程式解释气体变为浅棕色的原因___。
(2)乙同学分析“若OH-大量存在,NO![]() 也可能不大量存在”,重新设计实验证实如下:
也可能不大量存在”,重新设计实验证实如下:
装置 | 现象 |
| Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,有刺激性气味 |
为确认:"刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
产生该刺激性气味气体的离子方程式是___。
(3)甲、乙两位同学设计的实验初始时均未见明显现象的原因是___。
(4)根据以上实验分析,该溶液中一定大量存在的离子是___。