题目内容
【题目】M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:
(1)元素Q的名称为______________,P的基态原子价层电子排布式为__________________。
(2)O的氢化物的沸点比其上一周期同族元素的氢化物低,是因为___________________。
(3)M、O电负性大小顺序是__________(用元素符号表示),O的最高价含氧酸根的空间构型为_____________,其中心原子的杂化类型为_______________。
(4)M、N形成的化合物的晶胞如图所示,该晶胞的化学式为__________________,其中M离子的配位数为_____________,该晶体类型为____________________。
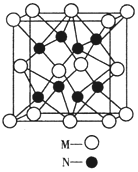
(5)该晶胞的边长为 a pm,则该晶体的密度为____________________g/cm3
【答案】锰 3d54s1 HF分子间存在氢键,而HCl分子间无氢键 O>Cl 正四面体 sp3 Na2O 8 离子晶体 ![]()
【解析】
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素。M原子最外层电子数为内层电子数的3倍,M原子只能有2个电子层,最外层电子数为6,则M为氧元素;N的焰色反应呈黄色,则N为Na;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质,可推知O为Cl、Q为Mn;P是一种金属元素,其基态原子中有6个未成对电子,核外电子排布为1s22s22p63s23p63d54s1,则P为Cr。据此分析解答。
根据上述分析,M为氧元素,N为Na元素,O为Cl元素,Q为Mn元素,P为Cr元素。
(1)元素Q为锰,P为Cr元素,处于第四周期,核外电子排布为1s22s22p63s23p63d54s1,价层电子排布式为3d54s1,故答案为:锰;3d54s1;
(2)HF分子间存在氢键,而HCl分子间无氢键,故HCl的沸点比HF的低,故答案为:HF分子间存在氢键,而HCl分子间无氢键;
(3)O、Cl元素形成的氧化物中Cl元素表现正化合价,故O原子对键合电子的吸引力更强,故电负性O>Cl,Cl的最高价含氧酸根为ClO4-,Cl原子孤电子对=![]() =0,价层电子对数为4,故其空间构型为正四面体,其中心原子的杂化类型为sp3,故答案为:O>Cl;正四面体;sp3;
=0,价层电子对数为4,故其空间构型为正四面体,其中心原子的杂化类型为sp3,故答案为:O>Cl;正四面体;sp3;
(4)晶胞中Na为晶胞内部,晶胞中含有8个Na原子,O原子位于顶点与面心,晶胞中含有O原子数目为8×![]() +6×
+6×![]() =4,故该晶胞的化学式为Na2O,以晶胞中上面心M离子为研究对象,晶胞中每个M周围最近的N离子有8个,M离子配位数为8,该晶体类型为离子晶体,故答案为:Na2O;8;离子晶体;
=4,故该晶胞的化学式为Na2O,以晶胞中上面心M离子为研究对象,晶胞中每个M周围最近的N离子有8个,M离子配位数为8,该晶体类型为离子晶体,故答案为:Na2O;8;离子晶体;
(5)晶胞的边长为apm,则晶胞的体积为(a×10-10)3cm3,晶胞中Na原子数目为8,O离子数目为8×![]() +6×
+6×![]() =4,所以晶胞的密度为
=4,所以晶胞的密度为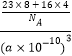 g/cm3=
g/cm3=![]() g/cm3,故答案为:
g/cm3,故答案为:![]() 。
。