题目内容
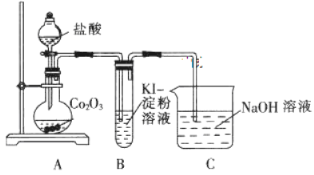
【题目】I.实验室常用的几种气体发生装置如图A、B、C所示。
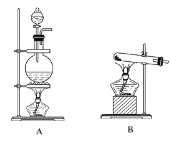
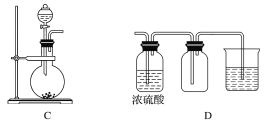
(1)实验室可以用B或C装置制取氨气,如果用C装置,通常使用的试剂是_________;
检查C装置的气密性是否良好的操作方法是____________________________。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是________(填序号,下同)。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
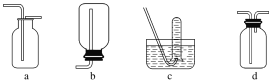
如图是某学生设计收集气体的几种装置,其中不可行的是________。
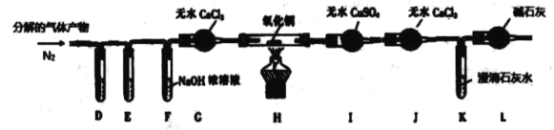
(3)若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的________。
①CO2 ②NO ③Cl2 ④H2
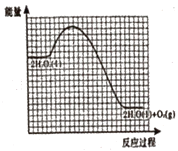
II.镁与稀硝酸的反应为:Mg+HNO3(稀)——Mg(NO3)2+NO↑+H2O(未配平)
(4)该反应中,还原产物是_________,HNO3表现了___________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
【答案】浓氨水和氧化钙(或碱石灰、固体氢氧化钠等) 关闭分液漏斗的活塞,将导气管通入水槽中,用手或热手巾捂圆底烧瓶,如果导气管处有气泡产生,松开手或拿去热毛巾后,导气管口形成一段稳定的液柱,则说明装置的气密性良好 ②④ b ③ NO 氧化性,酸性
【解析】
I.(1)实验室制取氨气常用Ca(OH)2与NH4Cl在加热条件下制备氨气或用浓氨水在CaO作用下制备氨气,前者需要加热,后者无需加热,如果用C装置,通常使用的药品是浓氨水和CaO;检查C装置气密性是否良好的操作方法是关闭分液漏斗的活塞,将导气管通入水槽中,用手或热手巾捂圆底烧瓶,如果导气管处有气泡产生,松开手或拿去热毛巾后,导气管口形成一段稳定的液柱,则说明装置的气密性良好;故答案为:浓氨水和氧化钙(或碱石灰、固体氢氧化钠等);关闭分液漏斗的活塞,将导管插入水中,用手捂住圆底烧瓶,看到气泡冒出,松开手后,在导管形成一段水柱,说明装置气密性良好;
(2)收集气体的方法的选择可依据气体的密度和溶解性,如气体与氧气反应则只能用排水法收集,气体是否有颜色与收集方法无关,与热稳定性无关;b装置由于气体进入后不能排出集气瓶的空气,所以b装置无法用于收集气体;故答案为:②④;b;
(3)若用A装置与D装置相连制取收集X气体,是固体液体加热制备的气体,气体不能和浓硫酸发生反应,密度比空气重,可以用向上排气法收集,且需进行尾气处理的气体,故:
①CO2制备不需要加热,二氧化碳气体无需尾气吸收装置,故①错误;
②NO 可以制备但不能用排空气法收集,故②错误;
③Cl2是固体和液体加热制备,用浓硫酸干燥,用向上排空气法收集,氯气有毒,不能直接排放到空气中,应有尾气吸收装置,故③正确;
④H2制备不需要加热,氢气比空气轻不能用向上排空气法收集,故④错误;
故答案为:③;
II.(4)该反应中,HNO3中的N元素由+5价转化为NO中的+2价,化合价降低被还原成还原产物,故还原产物是NO,此过程中HNO3表现了氧化性,但是还有部分HNO3中N的化合价并未改变,这部分硝酸则表现了酸性,故答案为:氧化性和酸性。