题目内容
【题目】如图:电流计的指针会偏转,M极变粗,N极变细符合这种现象的是
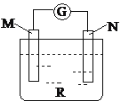
A. M是铜,N是锌,R是硫酸溶液
B. M是锌,N是铜,R是硫酸铜溶液
C. M是银,N是锌,R是硝酸银溶液
D. M是铁,N是铜,R是硝酸铜溶液
【答案】C
【解析】
M极变粗,N极变细,说明M极是正极,N极是负极,电解质溶液中的金属离子要在正极上被还原析出金属单质。
A.M极反应为2H++2e-==H2,无法析出金属单质,故A不符合;
B.锌比铜活泼作负极,M极变细,故B不符合;
C. N是锌,发生的反应为Zn-2e-==Zn2+,锌溶解,N极变细,M极发生的反应为Ag++e-==Ag,M极变粗,故C符合;
D.铁比铜活泼,为负极,发生反应Fe-2e-==Fe2+,M极变细,故D不符合。
本题选C。

【题目】Ⅰ、已知:N2(g)+3H2(g)![]() 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
450℃时,往一个2L的密闭容器中充入2. 6mol H2和1mol N2, 反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
c(NH3)/mol·L—1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
(1)此条件下该反应的化学平衡常数K=_______________;反应达到平衡后,若往平衡体系中加入H2、N2和NH3各2mol,此时该反应的v(N2)正____________v(N2)逆(填写“>”、“=”或“<”=)。
(2)若改变某一条件,达新平衡时n(H2)=1.60mol ,下列说法正确的是_____________。
A.平衡可能正向移动 B.可能是向容器中加入了一定量的H2气体
C.可能是降低了容器的温度 D.可能是增大了容器的体积
Ⅱ、已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
(1)若溶液中只溶解了一种溶质,该溶质的名称是__________,上述离子浓度大小顺序关系中正确的是(选填序号)_________________________。
(2)若上述关系中C是正确的,则溶液中溶质的化学式是______________
(3)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同)_____c(NH3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)______c(Cl-)。