题目内容
1. 原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素之一,Y的基态原子最外层电子数是其内层电子总数的2倍,Z的基态原子2p轨道上有3个未成对电子,W的原子序数为29.
原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素之一,Y的基态原子最外层电子数是其内层电子总数的2倍,Z的基态原子2p轨道上有3个未成对电子,W的原子序数为29.回答下列问题:
(1)上述元素能形成原子晶体单质的是C(填元素符号,下同),能形成金属晶体的是Cu.
(2)元素Y、Z组成的晶体具有空间网状结构,其化学式为C3N4,其硬度比晶体硅大(填“大”或“小”).
(3)一种由元素W与Au组成的合金晶体具有立方最密堆积结构.其晶胞中W原子处于面心,Au原子处于顶点位置,则该合金中W原子与Au原子数目之比为3:1,该晶体中,原子之间的作用力是金属键.该晶体具有储氢功能,氢原子可进入到由W原子与Au原子构成的四面体空隙中.若将W原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似(如图所示),该晶体储氢后的化学式为HxAuyCuz,x:y:z为H8AuCu3.
分析 Y的基态原子最外层电子数是其内层电子总数的2倍,最外层电子数为4,内层电子数为2,那么Y是C元素;
X是形成化合物种类最多的元素之一,那么X是H元素;
元素Z基态原子的2p轨道上有3个未成对电子,核外电子排布为1s22s22p3,则Z为N元素;
W的原子序数为29,那么W是Cu元素,
(1)C的单质易形成原子晶体,Cu为金属晶体;
(2)依据C元素和N元素在化合物中常见化合价判断即可;
(3)W的原子序数为29,则W是Cu元素,结合元素、物质的结构和性质分析解答.
解答 解:Y的基态原子最外层电子数是其内层电子总数的2倍,最外层电子数为4,内层电子数为2,那么Y是C元素;
X是形成化合物种类最多的元素之一,那么X是H元素;
元素Z基态原子的2p轨道上有3个未成对电子,核外电子排布为1s22s22p3,则Z为N元素;
W的原子序数为29,那么W是Cu元素,
(1)碳元素易形成原子晶体:金刚石,铜为金属晶体,故答案为:C;Cu;
(2)C元素在化合物中呈现+4价,N元素易形成-3价,故两者形成的化合物为:C3N4,由于C与N的半径比Si要小,故C-N键键能比Si-Si键能大,故硬度比晶体硅大,故答案为:C3N4;大;
(3)合金中原子之间存在金属键,Cu原子处于面心,Au原子处于顶点位置,该晶胞中Cu原子个数=6×$\frac{1}{2}$=3,Au原子个数=8×$\frac{1}{8}$=1,故Cu原子与Au原子数目之比为3:1,根据图知,黑色小球相当于H原子,为8个,所以晶体储氢后的化学式应为H8AuCu3,
故答案为:3:1;金属键;H8AuCu3.
点评 本题以元素的推断为载体,考查了晶体类型的判断、晶胞的计算等,难度中等,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
7.几种短周期元素的原子半径及主要化合价如表:下列叙述正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | R的氧化物对应的水化物可能具有两性 | |
| B. | X单质可在氧气中燃烧生成XO3 | |
| C. | 离子半径大小:r (M3+)>r (T2-) | |
| D. | L2+和X2-的核外电子数相等 |
12.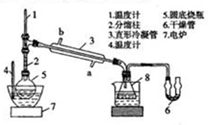 硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:
硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:
Na2B4O7•10H2O+2H2SO4+12CH3OH=2NaHSO4+4(CH3O)3B+17H2O
实验步骤:
在圆底烧瓶中加入44.8g甲醇和19.1gNa2B4O7•10H2O(硼砂,式量382)然后缓慢地加入浓H2SO4并振荡;用电炉加热烧瓶中的液体;回流一段时间后,先接收51~55℃的馏分,再接收55~60℃的馏分;两次所得馏分合并,加入氯化钙进行盐析分层,上层为硼酸三甲酯,分离;精馏得高纯硼酸三甲酯19.2g.
回答下列问题:
(1)图中仪器8的名称是锥形瓶,直形冷凝管冷却水应从a(填字母)接口进入.
(2)装有P2O3的干燥管作用是防止空气中水蒸气进入导致硝酸三甲酯水解.
(3)采用较高的甲醇与硼砂的物质的量之比的目的是提高硼砂的转化率.
(4)两次馏分中含硼酸三甲酯含量较高的是第1(填“1”或“2”)次.
(5)盐析后分离出硼酸三甲酯所需的主要玻璃仪器是分液漏斗.
(6)精馏时应收集68℃的馏分.
(7)本次实验的产率是D.
A.42.9% B.46.6% C.64.5% D.92.3%
 硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:
硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:Na2B4O7•10H2O+2H2SO4+12CH3OH=2NaHSO4+4(CH3O)3B+17H2O
| 硼酸三甲酯 | 甲醇 | |
| 相对分子量 | 104 | 32 |
| 溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
| 沸点/℃ | 68 | 64 |
| 备注 | 硼酸三甲酯与甲醇能形成共沸混合物,沸点54℃ | |
在圆底烧瓶中加入44.8g甲醇和19.1gNa2B4O7•10H2O(硼砂,式量382)然后缓慢地加入浓H2SO4并振荡;用电炉加热烧瓶中的液体;回流一段时间后,先接收51~55℃的馏分,再接收55~60℃的馏分;两次所得馏分合并,加入氯化钙进行盐析分层,上层为硼酸三甲酯,分离;精馏得高纯硼酸三甲酯19.2g.
回答下列问题:
(1)图中仪器8的名称是锥形瓶,直形冷凝管冷却水应从a(填字母)接口进入.
(2)装有P2O3的干燥管作用是防止空气中水蒸气进入导致硝酸三甲酯水解.
(3)采用较高的甲醇与硼砂的物质的量之比的目的是提高硼砂的转化率.
(4)两次馏分中含硼酸三甲酯含量较高的是第1(填“1”或“2”)次.
(5)盐析后分离出硼酸三甲酯所需的主要玻璃仪器是分液漏斗.
(6)精馏时应收集68℃的馏分.
(7)本次实验的产率是D.
A.42.9% B.46.6% C.64.5% D.92.3%
9.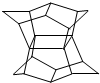 1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
 1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )| A. | 分子式为C20H20 | B. | 一氯代物的同分异构体只有四种 | ||
| C. | 分子中含有二个亚甲基(-CH2-) | D. | 分子中含有8个五元碳环 |
16.有八种物质:①甲烷、②苯、③聚乙烯、④乙烯、⑤2-丁炔、⑥环己烷、⑦邻二甲苯、⑧环己烯,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ②③④⑤⑧ | B. | ④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
6.在下列溶液中,各组离子一定能够大量共存的是( )
| A. | Cu2+、Mg2+、SO42- | B. | H+、Mg2+、CO32- | C. | Ag+、NO3-、Cl- | D. | Fe2+、H+、NO3- |
10.A、B、C、D是4种短周期元素,已知A、C同主族,B、C、D同周期,A的气态氢化物比C的气态氢化物稳定,B的阳离子比D的阳离子氧化性强,B的阳离子比C的阴离子少一个电子层.下列有关说法中,不正确的是( )
| A. | 原子序数 C>B>D>A | B. | 单质熔点 D>B,A>C | ||
| C. | 原子半径 D>B>C>A | D. | 简单离子半径 C>A>D>B |
 .
. .
. .
.