题目内容
【题目】关于水解应用的说法,错误的是
A.草木灰(主要含K2CO3)与铵态氮肥最好不混用
B.明矾用于净水
C.向CuCl2溶液中加入Cu(OH)2,调节pH可除去溶液中混有的少量Fe3+
D.将AlCl3、Al2(SO4)3溶液分别加热、蒸发、浓缩、结晶、灼烧,所得固体成分相同
【答案】D
【解析】
A.草木灰中![]() 和铵态氮肥中
和铵态氮肥中![]() 会发生相互促进的双水解反应生成不稳定的NH3H2O降低肥效,故A不符合题意;
会发生相互促进的双水解反应生成不稳定的NH3H2O降低肥效,故A不符合题意;
B.明矾中Al3+会发生水解生成Al(OH)3胶体,Al(OH)3胶体能够吸附水中的悬浮颗粒达到净水,故B不符合题意;
C.向CuCl2溶液中加入Cu(OH)2,调节pH,可促进Fe3++3H2OFe(OH)3+3H+正向进行,Cu2+几乎不发生沉淀,可除去溶液中混有的Fe3+,故C不符合题意;
D.由于盐酸易挥发,硫酸难挥发,所以将AlCl3、Al2(SO4)3溶液分别加热、蒸发、浓缩、结晶、灼烧,所得固体成分不相同,分别是氧化铝和硫酸铝,故D符合题意;
故答案为:D。

 芝麻开花课程新体验系列答案
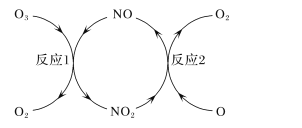
芝麻开花课程新体验系列答案【题目】I.亚硫酸钠的氧化反应:2Na2SO3 (aq) +O2(aq)=2Na2SO4(aq) H=x kJ/mol。其反应速率受溶解氧浓度影响,分为富氧区和贫氧区两个阶段。
(1)已知O2(g) ![]() O2(aq) H=y kJ/mol,Na2SO3 溶液与O2(g)反应的热化学方程式为___________________。
O2(aq) H=y kJ/mol,Na2SO3 溶液与O2(g)反应的热化学方程式为___________________。
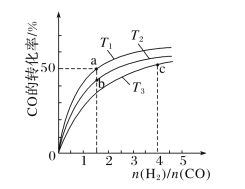
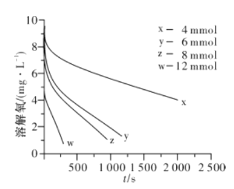
(2)291.5 K时,1.0 L溶液中Na2SO3初始量分别为4、6、8、12 mmol,溶解氧浓度初始值为9.60 mg/L,每5 s记录溶解氧浓度,实验结果如图所示。当Na2SO3初始量为12 mmol,经过20 s溶解氧浓度降为6.40 mg/L,则0~20s内Na2SO3的平均反应速率为_______mol/(L·s)。
(3)为确定贫氧区速率方程v=k·ca(SO32-)·cb(O2)中的a、b的值(取整数),分析实验数据。
c(Na2SO3)×103 | 3.65 | 5.65 | 7.65 | 11.65 |
v×106 | 10.2 | 24.4 | 44.7 | 103.6 |
①当溶解氧浓度为4.0 mg/L时,c(SO32-)与速率数值关系如表(甲)所示,则a=____。
②当溶解氧浓度小于4.0mg/L时,图中曲线皆为直线,Na2SO3氧化速率与溶解氧浓度无关,则b=_______。
(4)两个阶段不同温度的速率常数之比如表(乙)所示。已知![]() ,R为常数。Ea(富氧区)_____ (填“>”或“<”)Ea(贫氧区)。
,R为常数。Ea(富氧区)_____ (填“>”或“<”)Ea(贫氧区)。
反应阶段 | 速率方程 |
|
富氧区 | v=k·c (SO32-)·c (O2) | 1.47 |
贫氧区 | v=k·ca (SO32-)·cb(O2) | 2.59 |
II. (5)在容积固定的密闭容器中,起始充入0.2 mol SO2和0.1 mol O2,反应体系起始总压强0.1MPa。反应在一定温度下达到平衡时SO2的转化率为90%。该反应的压强平衡常数Kp=________ ( 分压=总压×物质的量分数)(写单位)。
(6)利用原电池原理,也可用SO2和O2来制备硫酸,该电池用多孔材料作电极。请写出该电池负极反应式_________________________。
【题目】下列有关化学实验操作,现象和结论均为正确的是
选项 | 操作 | 现象 | 结论 |
A | Mg2+和Cu2+共存的溶液中滴入适量NaOH溶液 | 产生白色沉淀 | 相同温度下,溶度积常数 Ksp[Mg(OH)2]<Ksp[Cu(OH)2] |
B | 加热盛有(NH4)2CO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 试纸变蓝 | (NH4)2CO3显碱性 |
C | 常温下,向等浓度、等体积的Na2CO3和NaHCO3溶液中滴加等量的酚酞溶液 | 碳酸钠溶液中红色更深 | 阴离子水解常数Kh: CO32->HCO3- |
D | 向饱和硼酸溶液中滴加少量Na2CO3粉末 | 无气泡冒出 | 不能证明酸性:碳酸>硼酸 |
A.AB.BC.CD.D