题目内容
【题目】常温常压下,将NH3缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入CO2,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发)。下列叙述不正确的是
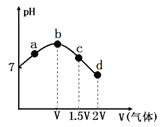
A.由a点到b点的过程中,溶液中 增大
增大
B.由图可知(NH4)2CO3溶液显碱性、NH4Cl溶液显酸性
C.c点所示溶液中,c(NH4+)>c(CO32-)>c(OH-)>c(H+)
D.d点所示溶液中,c(NH4+)+c(NH3·H2O)=c(HCO3-)+c(CO32-)+c(H2CO3)
【答案】D
【解析】
A. ,由a点到b点,溶液pH增大,c(OH-)增大,由于温度不变,Ka不变,因此
,由a点到b点,溶液pH增大,c(OH-)增大,由于温度不变,Ka不变,因此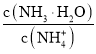 增大,A正确;
增大,A正确;
B. b点表示NH3的量达到最大值,c点时,溶液中的一水合氨和二氧化碳恰好完全反应,溶质为碳酸铵,由图可知(NH4)2CO3溶液显碱性、NH4Cl溶液显酸性,B正确;
C.c点所示溶液中,溶质为碳酸铵,溶液呈碱性,因此离子浓度大小为:c(NH4+)>c(CO32-)>c(OH-)>c(H+),C正确;
D. d点所示溶液中,溶质为碳酸氢铵,根据质子守恒可知,c(NH4+)+c(NH3·H2O)+ c(NH3)=c(HCO3-)+c(CO32-)+c(H2CO3),D错误。
故答案D。

练习册系列答案
相关题目