题目内容
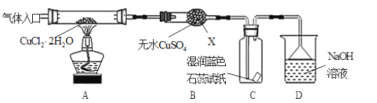
【题目】固体粉末 X 中可能含有 Fe2O3、CuO、MnO2、CaO、NaCl 和 K2CO3 中的若干种。为确定该固体粉末的成分,进行了以下实验(所加试剂均过量):

下列结论正确的是:
A. 固体粉末中一定含 K2CO3B. X 中可能存在 Fe2O3
C. 沉淀 M 一定含 AgClD. 沉淀 Y 中不一定存在 MnO2
【答案】B
【解析】
A.固体粉末X中加入水,有难溶性的固体Y,也有可溶性的液体Z,该溶液显碱性,可能是CaO溶于水,与水反应产生的Ca(OH)2电离导致,也可能是 K2CO3 水解使溶液显碱性,A不合理;
B.若固体粉末 X 中含有 Fe2O3,该物质不溶于水,向其中加入盐酸,发生反应产生FeCl3和水,该盐的水溶液显黄色,从而得到有色溶液,B正确;
C.向溶液Z中加入AgNO3溶液,产生沉淀M,可能是Ag2CO3,也可能是AgCl,C错误;
D.向不溶于水的固体中加入浓盐酸,发生反应,产生黄绿色气体,是由于发生反应:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,可以证明沉淀 Y 中一定存在MnO2,D错误;
MnCl2+Cl2↑+2H2O,可以证明沉淀 Y 中一定存在MnO2,D错误;
故合理选项是B。

练习册系列答案
相关题目
【题目】下列实验中,实验现象及结论都正确且两者具有因果关系的是
实验 | 现象 | 结论 | |
A | 向Ba(NO3)2溶液中通入二氧化硫气体 | 有白色沉淀生成 | SO2与Ba(NO3)2反应得到BaSO3 |
B | 向FeI2的溶液中滴加少量的氯水 | 溶液颜色变深 | Cl2与Fe2+反应生成Fe3+ |
C | 向蔗糖溶液中加几滴稀硫酸,水浴加热5min后,再加新制Cu(OH)2后加热 | 无砖红色沉淀生成 | 蔗糖没有水解 |
D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
A. A B. B C. C D. D