题目内容
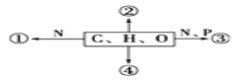
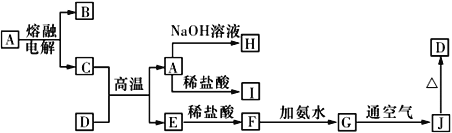
【题目】A~J是中学化学常见的物质,它们之间的转化关系如下图所示 (部分反应条件、生成物已省略)。已知A是一种高熔点物质,D是一种红棕色固体。
请回答下列问题:
(1)电解A物质的阴极电极反应式为________,C与D在高温下反应,引发该反应需要加入的两种试剂是________________________(填名称)。
(2)写出G→J反应的实验现象与化学方程式:____________________________,________________________________。
(3)C与NaOH溶液反应的离子方程式为________________________________。
【答案】 A13++3e-=Al 镁带、氯酸钾 白色沉淀迅速变为灰绿色,最终变为红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3 2Al+2OH-+2H2O==2AlO2-+3H2↑
【解析】试题分析:由题意知,A是氧化铝、D是氧化铁,由图中转化关系,可以推断B是氧气、C是铝、E是铁、F是氯化亚铁、G是氢氧化亚铁、H是偏铝酸钠、I是氯化铝或氢气、J是氢氧化铁。
(1)电解A物质的阴极电极反应式为A13++3e-=Al,C与D在高温下反应,该反应为铝热反应,引发该反应需要加入的两种试剂是镁带、氯酸钾。
(2)G→J反应的实验现象为白色沉淀迅速变为灰绿色,最终变为红褐色;访反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(3)C与NaOH溶液反应的离子方程式为2Al+2OH-+2H2O==2AlO2-+3H2↑。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
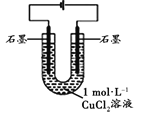
冲刺100分单元优化练考卷系列答案【题目】某小组同学利用下图装置对电解氯化铜实验进行了研究。
装置 | 现象 |
| 电解一段时间时,阳极石墨表面产生气体,阴极石墨上附着红色物质,烧杯壁变热,溶液由蓝色变为绿色 |
(1)甲认为电解过程中阳极产生的_________是溶液变绿的原因。
(2)乙查阅资料,CuCl2溶液中存在平衡:Cu2+ + 4Cl-![]() [CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:________________。
[CuCl4]2-(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2-(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2-浓度增大的原因:________________。
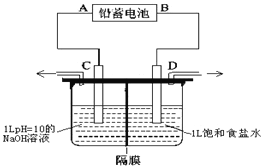
(3)丙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
装置 | 现象 |
| 电解相同时间时,阳极石墨表面产生气泡,溶液仍为蓝色;阴极石墨上附着红色物质,溶液由蓝色变为绿色;U型管变热,冷却后阴极附近溶液仍为绿色 |
丙通过对现象分析证实了甲和乙的观点均不是溶液变绿的主要原因。丙否定甲的依据是________,否定乙的依据是________________。
(4)丙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]-,[CuCl2]-掺杂Cu2+后呈黄色
ii. 稀释含[CuCl2]-的溶液生成CuCl白色沉淀据此丙认为:电解过程中,产生[CuCl2]-掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
丙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]-的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是__________________。
② 写出b中生成[CuCl2]-的离子方程式:____________________。
③ 补充c中必要的操作及现象:____________________。
丙据此得出结论:电解时阴极附近生成[CuCl2]-是导致溶液变绿的原因。
【题目】在2L恒容密闭容器中加入0.100molNO和2.030mol固体活性炭,发生反应:2NO(g)+C(s) ![]() N2(g)+CO2(g)。在不同温度下测得平衡体系中各物质的物质的量如下表,下列说法正确的是
N2(g)+CO2(g)。在不同温度下测得平衡体系中各物质的物质的量如下表,下列说法正确的是
温度 | C(s)/mol | NO/mol | N2/mol | CO2/mol |
200℃ | 2.000 | 0.0400 | 0.0300 | 0.0300 |
335℃ | 2.005 | 0.0500 | 0.0250 | 0.0250 |
A. 该反应的正反应为吸热反应
B. 反应体系在335℃时的平衡常数为0.25
C. 335℃与200℃时相比,活化分子个数、活化分子百分数、活化能及焓变均大
D. 200℃时,平衡后向恒容容器中再充入0.10molNO,再次平衡时,NO的百分含量将增大