题目内容
【题目】(1)将4gNaOH固体溶于水配成250mL溶液,此溶液中NaOH的物质的量浓度为___mol/L。取出10mL此溶液,其中含有NaOH_____g。将取出的溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为______mol/L。
(2)如图实验室某浓盐酸试剂瓶标签上的有关数据,据此计算:该浓盐酸中HCl的物质的量浓度为______mol/L;用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸。需要量取______mL上述浓盐酸进行配制。

(3)100mL0.3mol/LNa2SO4溶液和50mL0.2mol/LAl2(SO4)3溶液混合后,溶液中SO42-的物质的量浓度为_______mol/L。
(4)标准状况下,将V L A气体(摩尔质量为M g/mol)溶于0.1L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为__________mol/L。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】0.40.160.0411.916.80.4B
【解析】
(1)将4gNaOH固体溶于水配成250mL溶液,氢氧化钠的物质的量是4g÷40g/mol=0.1mol,则此溶液中NaOH的物质的量浓度为0.1mol÷0.25L=0.4mol/L。取出10mL此溶液,其中含有NaOH的质量是0.01L×0.4mol/L×40g/mol=0.16g。将取出的溶液加水稀释到100mL,由于稀释过程中溶质的物质的量不变,则稀释后溶液中NaOH的物质的量浓度为![]() =0.04mol/L。
=0.04mol/L。
(2)根据![]() 可知该浓盐酸中HCl的物质的量浓度为
可知该浓盐酸中HCl的物质的量浓度为![]() =11.9mol/L;由于稀释过程中溶质的物质的量不变,则用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸,需要量取上述浓盐酸的体积为
=11.9mol/L;由于稀释过程中溶质的物质的量不变,则用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸,需要量取上述浓盐酸的体积为![]() 。
。
(3)100mL0.3mol/LNa2SO4溶液和50mL0.2mol/LAl2(SO4)3溶液混合后,溶液中SO42-的物质的量浓度为![]() 。
。
(4)标准状况下,将V L A气体(摩尔质量为M g/mol)溶于0.1L水(密度1 g/cm3)中,溶质的物质的量是![]() ,质量是
,质量是![]() ,溶液质量是100g+
,溶液质量是100g+![]() ,所得溶液的密度为d g/mL,则此溶液的体积为
,所得溶液的密度为d g/mL,则此溶液的体积为![]() ,所以溶液的物质的量浓度为
,所以溶液的物质的量浓度为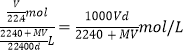 ,答案选B。
,答案选B。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案