题目内容
【题目】室温时,两个容积相同的烧瓶中分别盛有下面两种气体(同温同压),打开弹簧夹K,使两烧瓶内的气体充分混合后,容器内的压强最小的是
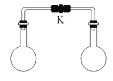
A.H2S和 SO2B.NH3和HCl
C.H2和Cl2D.NO和 O2
【答案】B
【解析】
假设每个烧瓶盛有2mol的气体,
A.打开弹簧夹K,发生反应2H2S+SO2=3S↓+H2O,最后剩余1molSO2气体;
B.打开弹簧夹K,发生反应NH3+HCl= NH4Cl,两者恰好完全反应生成氯化铵固体,装置内无气体剩余;
C.H2和Cl2在常温常压条件下不反应,剩余的还是4mol气体;
D.打开弹簧夹K,发生反应2NO+O2= 2NO2,若不考2NO2N2O4,装置内剩余3mol的气体,考虑到可逆反应2NO2N2O4,剩余的气体在2mol~3mol之间;
恒温恒容下,气体的压强之比等于气体物质的量之比,B中的压强最小,答案选B。

练习册系列答案
相关题目