题目内容
下列各组物质相互反应时,产生的气体能燃烧的是( )
| A、碳化钙[CaC2]投入水中 |
| B、炽热的焦炭投入浓硝酸中 |
| C、少量的二氧化锰加入双氧水中 |
| D、乙醇和浓硫酸共热至170℃ |
考点:硝酸的化学性质,过氧化氢,浓硫酸的性质
专题:元素及其化合物
分析:A.碳化钙[CaC2]投入水中生成C2H2具有可燃性;
B.二氧化碳和二氧化氮没有可燃性;
C.少量的二氧化锰加入双氧水中产生的氧气不能燃烧;
D.乙醇和浓硫酸共热到170℃生成乙烯,乙烯具有可燃性.
B.二氧化碳和二氧化氮没有可燃性;
C.少量的二氧化锰加入双氧水中产生的氧气不能燃烧;
D.乙醇和浓硫酸共热到170℃生成乙烯,乙烯具有可燃性.
解答:
解:A.碳化钙[CaC2]投入水中反应CaC2+2H2O=Ca(OH)2+C2H2↑,生成C2H2具有可燃性,故A正确;
B.浓硝酸和炽热的碳反应C+4HNO3(浓)
CO2↑+4NO2↑+2H2O生成二氧化碳和二氧化氮、水,没有可燃性气体生成,故B错误;
C.少量的二氧化锰加入双氧水中2H2O2
2H2O+O2↑,生成氧气,氧气不能燃烧但能助燃,故C错误;
D.乙醇和浓硫酸共热到170℃CH3CH2OH
CH2=CH2↑+H2O生成乙烯,乙烯具有可燃性,故D正确;
故选AD.
B.浓硝酸和炽热的碳反应C+4HNO3(浓)
| ||
C.少量的二氧化锰加入双氧水中2H2O2
| ||
D.乙醇和浓硫酸共热到170℃CH3CH2OH
| 浓硫酸 |
| 170℃ |
故选AD.
点评:本题考查气体的性质,明确发生的化学反应及反应中气体的性质是解答本题的关键,注意氧气没有可燃性,但能助燃.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
X、Y、Z三种元素,已知X和Y原子核外电子层数相同,Y和Z原子最外层电子数相同,又知三种元素原子最外层电子数总和为14,而质子数总和为28,则三种元素为( )
| A、N、P、O |
| B、N、C、Si |
| C、B、Mg、Al |
| D、C、N、P |
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加,计算电极d上生成的气体,在标准状态下体积是( )升.
| A、2.8 | B、5.6 |
| C、8.4 | D、11.2 |
门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确.根据元素周期律,下列有关X的性质的描述中正确的是( )
| A、X单质易与水反应 |
| B、X形成的氧化物易与水反应生成酸 |
| C、X易形成氧化物XO |
| D、XH4的稳定性比SiH4的低 |
同主族元素所形成的同一类化合物,其结构和性质往往相似,化合物PH4I是一种无色晶体,下列对它的描述中错误的是( )
| A、它是共价化合物 |
| B、在加热时,它能分解 |
| C、它能跟碱发生反应 |
| D、它可由PH3和HI化合而成 |
在密闭容器中一定量混合气体发生反应:x A(g)+y B(g)?z C(g),平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积压缩到原来的
,再达平衡时测得A的浓度为0.8mol/L,下列判断正确的是( )
| 1 |
| 2 |
| A、x+y<z |
| B、平衡向正反应方向移动 |
| C、B的物质的量增大 |
| D、C的体积分数保持不变 |
一定量的甲烷燃烧后生成CO、CO2、H2O(气),此混合气重49.6克,当其缓慢通过无水氯化钙时,氯化钙增重25.2克,原混合气中CO2的质量为( )
| A、12.5 克 |
| B、13.2克 |
| C、19.7克 |
| D、24.4克 |
直接NaBH4/H2O2燃料电池(DBFC)的结构如图,有关该电池的说法不正确的是( )
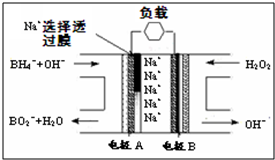

| A、电极B材料中包含MnO2层,MnO2可起催化作用 |
| B、电池负极区电极反应:BH4-+8OH--8e-═BO2-+6H2O |
| C、放电过程中,Na+从正极区向负极区迁移 |
| D、在电池反应中,每消耗1L 6mol/L H2O2溶液,理论上流过电路中的电子为12NA个 |
 某有机物X的分子结构如图所示,请回答下列问题:
某有机物X的分子结构如图所示,请回答下列问题: