题目内容
16.查阅元素周期表,从每个方格中不能得到的信息是( )| A. | 相对原子质量 | B. | 元素名称 | C. | 原子序数 | D. | 同位素种类 |
分析 如 ,在方格中可知元素名称为铝、原子序数为13、相对原子质量为26.98,以此来解答.
,在方格中可知元素名称为铝、原子序数为13、相对原子质量为26.98,以此来解答.
解答 解:元素周期表中每个方格中可知元素的名称、左上角的数值为原子序数,元素名称下方为相对原子质量,不能得到的信息为同位素种类,
故选D.
点评 本题考查元素周期表的应用,为基础性习题,把握周期表中方格内的信息为解答的关键,注重基础知识的夯实,题目难度不大.

练习册系列答案
相关题目
11.原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1.下列有关X的说法中不正确的是( )
| A. | X能与某些非金属元素化合 | |
| B. | X可能为金属元素 | |
| C. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| D. | X可能形成化学式为KXO3的盐 |
8.下列各反应的化学方程式中,不正确的是( )
| A. | 将点燃的镁条伸入充满CO2气体的集气瓶中:2Mg+CO2═点燃 2MgO+C | |
| B. | 大理石溶于醋酸:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O | |
| C. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O | |
| D. | 向淀粉KI溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H++4I-+O2═2I2+2H2O |
5.恒温下2HI(g)?H2(g)+I2(g)分解达到平衡,改变下列条件能引起平衡移动的是( )
| A. | 缩小容器的容积 | B. | 使用催化剂 | C. | 恒压下充入He | D. | 恒容下充入Cl2 |

 .
.

 .
.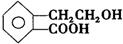 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.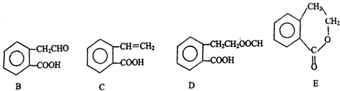
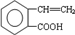 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ .
.