题目内容
【题目】对于0.1molL﹣1 NH4Cl溶液,正确的是( )
A.升高温度,溶液pH升高
B.通入少量HCl,c(NH4+)和c(Cl﹣)均增大
C.c(NH4+)+c(OH﹣)=c(Cl﹣)+c(H+)
D.c(Cl﹣)>c(H+)>c(NH4+)>c(OH﹣)
【答案】B
【解析】解:A.升高温度促进水解,NH4Cl水解,氢离子浓度增大,溶液pH降低,故A错误;
B.氢离子抑制氯化铵的水解,铵根浓度增大,加入了氯化氢,氯离子浓度增大,故B正确;
C.氯化铵不水解,铵根浓度与氢氧根相等,铵根水解,铵根浓度减少,氢离子浓度增大,故C错误;
D.水解程度很微弱,氢离子浓度小于铵根浓度,故D错误.
故选B.

【题目】中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如下图所示。
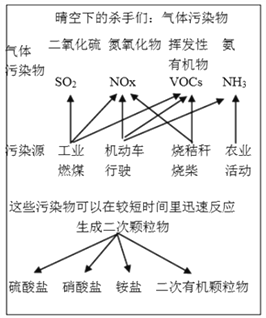
(1)根据上图信息可以看出,下列哪种气体污染物不是由机动车行驶造成的_______________。
a.SO2 b.NOx c.VOCs d. NH3
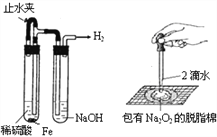
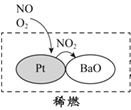
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式_______________。
(3)科学家经过研究发现中国霾呈中性,其主要原因如下图所示:
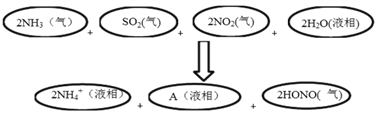
请判断A的化学式并说明判断理由:_____________________________________________。
(4)煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
离子 | Na+ | SO42 | NO3 | H+ | Cl |
浓度/(mol·L1) | 5.5×103 | 8.5×104 | y | 2.0×104 | 3.4×103 |
①SO2和NaClO2溶液反应的离子方程式是________________________________________。
②表中y =_______________。