题目内容
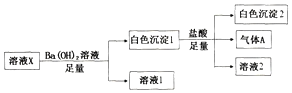
【题目】过氧硫酸氢钾复合盐(K2SO4KHSO42KHSO5)易分解,可用作漂白剂、NOx和SO2等的脱除剂。某研究小组制备过氧硫酸氢钾复合盐的流程如图所示。

已知:浓硫酸与H2O2反应,部分转化为过硫酸(化学式为H2SO5,是一种一元强酸)
(1)H2SO5中硫元素的化合价为+6价,其中过氧键的数目为________;工业上用过氧硫酸氢钾复合盐溶液脱除NO时,反应的离子方程式为___________________________。
(2)若反应物的量一定,在上述流程的“转化”步骤中需用冰水浴冷却,且缓慢加入浓硫酸,其目的是___________________________。
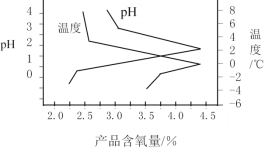
(3)“结晶”操作中,加入K2CO3即可获得过氧硫酸氢钾复合盐晶体,该过程的化学方程式为______________________________。过氧硫酸氢钾复合盐产率(以产品含氧量表示)随溶液pH和温度的变化关系如图所示,则该过程适宜的条件是_________________。
(4)产品中KHSO5含量的测定:取1.000g产品于锥形瓶中,用适量蒸馏水溶解,加入5mL5%的硫酸和5mL25%的KI溶液,再加入1mL淀粉溶液作指示剂,用0.2000mol·L-1硫代硫酸钠标准液滴定至终点,消耗标准液的体积为25.00mL。
已知:2KHSO5+4KI+H2SO4 = 2I2+3K2SO4+2H2O I2+2Na2S2O3 =Na2S4O6+2NaI
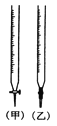
①用_____滴定管盛装标准浓度的硫代硫酸钠溶液(填“甲”或“乙”)。
②产品中KHSO5的质量分数为___________。
【答案】1 3HSO5-+2NO+H2O = 3SO42-+2NO3-+5H+ 防止浓硫酸与H2O2溶液混合时放出大量热使H2O2分解 5K2CO3+4H2SO5+4H2SO4 =2(K2SO4KHSO42KHSO5)↓+5CO2↑+5H2O 控制pH在2.0~2.5之间,温度在0℃左右 乙 38.00%
【解析】
(1)H2SO5中硫元素的化合价为+6价,依据化合价的代数和为0计算,有2个氧原子显-1价,所以过氧键的数目为1。答案为1;
工业上用过氧硫酸氢钾复合盐溶液脱除NO时,反应的离子方程式为3HSO5-+2NO+H2O = 3SO42-+2NO3-+5H+。答案为3HSO5-+2NO+H2O = 3SO42-+2NO3-+5H+
(2)在“转化”步骤中,30%的H2O2溶液加入98%的浓硫酸中,相当于浓硫酸稀释,会放出大量的热,而H2O2受热易分解,所以需用冰水浴冷却,且缓慢加入浓硫酸。
答案为:防止浓硫酸与H2O2溶液混合时放出大量热使H2O2分解;
(3)“结晶”操作中,加入K2CO3即可获得过氧硫酸氢钾复合盐晶体,该过程的化学方程式为5K2CO3+4H2SO5+4H2SO4 =2(K2SO4KHSO42KHSO5)↓+5CO2↑+5H2O。
答案为:5K2CO3+4H2SO5+4H2SO4 =2(K2SO4KHSO42KHSO5)↓+5CO2↑+5H2O
从溶液pH看,过氧硫酸氢钾复合盐产率在2.0~2.5之间时最大;从温度看,过氧硫酸氢钾复合盐产率在0℃左右最大,所以该过程适宜的条件是控制pH在2.0~2.5之间,温度在0℃左右。答案为:控制pH在2.0~2.5之间,温度在0℃左右;
(4) ① 硫代硫酸钠溶液呈碱性,应放在碱式滴定管内。答案为乙;
② 由反应2KHSO5+4KI+H2SO4 = 2I2+3K2SO4+2H2O和I2+2Na2S2O3 =Na2S4O6+2NaI可得出如下关系式:KHSO5——2Na2S2O3
n(Na2S2O3)=0.2mol/L×0.025L=0.005mol,n(KHSO5)=0.0025mol
产品中KHSO5的质量分数为:![]()
答案为:38.00%。