题目内容
从海水(含氯化镁)中提取镁,涉及如下步骤:
①将沉淀物与盐酸反应,结晶、过滤 ②在HCl气体氛围中干燥产物
③过滤、洗涤沉淀物 ④将得到的产物熔融电解得到镁
⑤把贝壳制成石灰乳[Ca(OH)2],在引入的海水中加入石灰乳,沉降。
下列说法正确的是:
①将沉淀物与盐酸反应,结晶、过滤 ②在HCl气体氛围中干燥产物
③过滤、洗涤沉淀物 ④将得到的产物熔融电解得到镁
⑤把贝壳制成石灰乳[Ca(OH)2],在引入的海水中加入石灰乳,沉降。
下列说法正确的是:
| A.正确操作步骤的顺序是⑤②③①④ |
| B.步骤④电解时阴极产生氯气 |
| C.直接在空气中将MgCl2溶液蒸干可得到Mg(OH)2高网 |
| D.此法提取镁的过程中涉及置换、分解、化合和复分解反应资 |
C
略

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
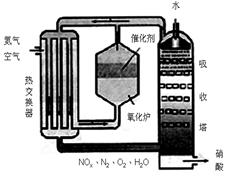
 4NO(g)+6H2O(l) △H<0
4NO(g)+6H2O(l) △H<0 2NH3(g) △H=" -92.4KJ/mol " ,据此回答以下问题:
2NH3(g) △H=" -92.4KJ/mol " ,据此回答以下问题:
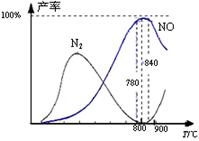
 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
 -1
-1 重,得到ZnO 2.43g和标准状况下CO20.224l,碱式碳酸锌的化学式
重,得到ZnO 2.43g和标准状况下CO20.224l,碱式碳酸锌的化学式