题目内容
【题目】下列关于实验室制氯气的说法中错误的是( )
A.该反应是一个氧化还原反应,其中二氧化锰是氧化剂
B.每生成1mol氯气,就要转移2mol电子
C.该反应的离子方程式为MnO2+4H++4Cl-![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.该方法是瑞典化学家舍勒最先发现的
【答案】C
【解析】
实验室制取氯气的离子方程式为:MnO2+4H++4Cl-![]() MnCl2+2H2O+Cl2↑,反应中氯元素化合价由-1价升高到0价,氯化氢作还原剂;锰元素化合价由+4价降低到+2价,二氧化锰作氧化剂;
MnCl2+2H2O+Cl2↑,反应中氯元素化合价由-1价升高到0价,氯化氢作还原剂;锰元素化合价由+4价降低到+2价,二氧化锰作氧化剂;
A. 该反应是一个氧化还原反应,其中二氧化锰是氧化剂,故A正确;
B. 每生成1mol氯气,转移电子为:1mol×2×[0-(-1)]=2mol,故B正确;
C. 氯化锰是可溶性的盐,故该反应的离子方程式为:MnO2+4H++4Cl-![]() MnCl2+2H2O+Cl2↑,故C错误;
MnCl2+2H2O+Cl2↑,故C错误;
D. 该方法是瑞典化学家舍勒最先发现的,故D正确;
答案选C。

【题目】某研究性学习小组的同学在学习了二氧化碳与过氧化钠的反应后,对过氧化钠与二氧化硫的反应进行实验探究。
(1)提出假设:
假设1. 固体产物是Na2SO3
假设2. _________________________
假设3. 固体产物是Na2SO3和Na2SO4的混合物。
(2)实验验证:用如图所示装置对上述假设进行实验。
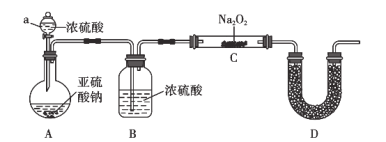
(1)仪器a的名称为__________,装置A中发生反应的化学方程式为:________________________。
(2)装置B的作用为________________________,装置D中试剂的名称为________。
(3)装置C中固体完全反应后,得到白色固体,进行如下实验。
实验操作 | 预期现象与结论 |
步骤1.取少量白色固体于试管中,加入足量的稀盐酸,将生成的气体通入品红溶液。 | 若_____________,说明白色固体中含有Na2SO3。 |
步骤2.在步骤1反应后的溶液中加入________ | 若_____________,说明白色固体中含有Na2SO4。 |
通过实验探究发现上述两个实验现象均有,则说明假设3正确。