题目内容
8.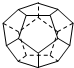 德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成(如图).请回答:C20分子共有12个正五边形,共有30条棱边,C20晶体属于分子晶体 (填晶体类型).
德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成(如图).请回答:C20分子共有12个正五边形,共有30条棱边,C20晶体属于分子晶体 (填晶体类型).
分析 每个顶点上碳原子被3个正五边形共用,则每个正五边形含有C原子个数=$\frac{1}{3}×5$=$\frac{5}{3}$;每个碳原子连接3个C-C单键,则每个碳原子含有C-C单键个数=$\frac{1}{2}×3$=$\frac{3}{2}$,根据物质的构成微粒判断晶体类型.
解答 解:每个顶点上碳原子被3个正五边形共用,则每个正五边形含有C原子个数=$\frac{1}{3}×5$=$\frac{5}{3}$,则正五边形个数=$\frac{20}{\frac{5}{3}}$=12;每个碳原子连接3个C-C单键,则每个碳原子含有C-C单键个数=$\frac{1}{2}×3$=$\frac{3}{2}$,则棱边个数=$\frac{3}{2}×$20=30,该晶体的构成微粒是分子C20,所以属于分子晶体,
故答案为:12;30;分子晶体.
点评 本题考查晶胞计算,侧重考查学生分析计算及空间想象能力,采用均摊法分析解答即可,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.同一周期三种非金属元素X、Y、Z,其最高价氧化物的水化物的酸性由强到弱的顺序是:HXO4>H2YO4>H3ZO4.下列说法正确的是( )
| A. | 元素的非金属性:X<Y<Z | B. | X、Y、Z依次位于ⅤA族、ⅥA族、ⅦA族 | ||
| C. | 阴离子的还原性:X->Y2->Z3- | D. | 气态氢化物的稳定性:HX>H2Y>ZH3 |
16.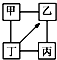 图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )
图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )
 图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )
图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | H2SO4 | Na2SO4 | NaOH | NaCl |
| B | KCl | K2CO3 | KOH | HCl |
| C | O2 | CO | CuO | C |
| D | Fe | CuCl2 | Zn | HCl |
| A. | A | B. | B | C. | C | D. | D |
3.荧光素是发光物质的基质,5-羧基荧光素与5-羧基荧光素二乙酸酯在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等.下列说法正确的是( )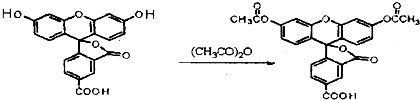
5-羧基荧光素(5-FAM) 5-羧基荧光素二乙酸酯(5-CFDA)
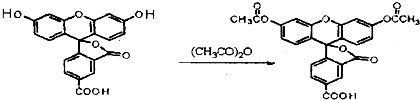
5-羧基荧光素(5-FAM) 5-羧基荧光素二乙酸酯(5-CFDA)
| A. | 5-FAM转变为5-CFDA属于取代反应 | |
| B. | 实验室鉴别5-FAM与5-CFDA可用碳酸氢钠溶液 | |
| C. | 5-FAM的分子式为:C21H3O7 | |
| D. | 5-FAM和5-CFDA分子中的所有原子均共面 |
13.仅用一种试剂便可以将苯、苯酚、四氯化碳、乙醛等4种无色液体进行鉴别,这种试剂是( )
| A. | 银氨溶液 | B. | 新制的氢氧化铜 | C. | 溴水 | D. | 氢氧化钠溶液 |
17.下列说法正确的是 ( )
| A. | 同一主族元素,原子半径越大,其单质的熔点不一定越高 | |
| B. | 全部由非金属元素组成的化合物中一定只有共价键 | |
| C. | 在由锌片、铜片、稀硫酸组成的原电池中,电子由铜片经外电路流向锌片 | |
| D. | 氯化钠和氯化氢分别溶解在水中所克服的粒子间相互作用属于同种类型 |
18.下列叙述正确的是( )
| A. | 稀硝酸、稀硫酸均能将木炭氧化成二氧化碳 | |
| B. | Na2O2与水反应,红热的Fe与水蒸气反应均能生成气体 | |
| C. | Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物 | |
| D. | NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
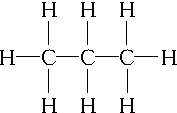 ,C3H6的同分异构体为CH2═CH-CH3、
,C3H6的同分异构体为CH2═CH-CH3、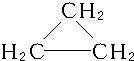 .
.