��Ŀ����
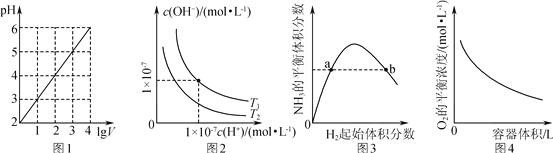
����Ŀ��T�����ֱ���10mlŨ�Ⱦ�Ϊ1mol/L����������HA��HB�в��ϼ�ˮϡ�ͣ�����pH�������ⶨ��ҺpH��������ҺpH������(2pH)����ҺŨ�ȵĶ���(1gc)�Ĺ�ϵ��ͼ��ʾ������������ȷ����
��֪����1��HA�ĵ���ƽ�ⳣ��Ka=[c(H+)��c(A-)]/[c(HA)-c(A-)]��c2(H+)/c(HA)����2��pKa=-lgKa

A. �����Ka����ҺŨ�ȵĽ��Ͷ�����
B. a���Ӧ����Һ��c(HA)=0.1mol/L��pH=4
C. ������HA<HB
D. ����HB��pKa=5
���𰸡�B
��������KaΪ�¶ȵĺ������¶Ȳ��䣬Ka�Ͳ�����A������a���Ӧ����Һ��1gc=-1���� c(HA)=0.1mol/L����Ӧ��pH=4��B��ȷ��ͨ��ͼ��������������Ũ�����ʱ��HA��Һ��pHС��HB��Һ��pH����������HA>HB��C����������ͼ������1gc=0ʱ��c(HB)=1mol/L, c(H+)=1��10-5mol/L��HB�ĵ���ƽ�ⳣ��Ka=c2(H+)/c(HB)=��1��10-5��2/1=1��10-10, pKa=-lgKa=-lg��10-10=10��D��������ȷѡ��B��

����Ŀ����(Te)Ϊ��VIAԪ�أ��䵥��ƾ�����������ܳ�Ϊ�����Ͻ����Ӽ����뵼�塢���Ԫ����������ϣ������㷺Ӧ����ұ�𡢺��պ��졢���ӵ����ɴӾ���ͭ��������(��Ҫ�ɷ�ΪCu2Te)�л����ڣ�
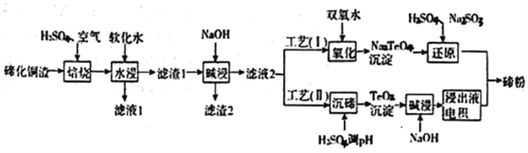
��1������������,ȷ��Ҫ��TeO2��ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ:________________________��
��2��Ϊ��ѡ����ѵ����չ��ս������¶Ⱥ�������������������飬������±���ʾ:
�¶�/�� | ���������(����������) | ������/% | |
Cu | Te | ||
450 | 1.25 | 77.3 | 2.63 |
460 | 1.00 | 80.29 | 2.81 |
1.25 | 89.86 | 2.87 | |
1.50 | 92.31 | 7.70 | |
500 | 1.25 | 59.83 | 5.48 |
550 | 1.25 | 11.65 | 10.63 |
��ʵ����Ӧѡ�������Ϊ_________________��ԭ��Ϊ______________________________��
��3������1�ڼ��ʱ�����Ļ�ѧ����ʽΪ_____________________________��
��4��������I���У�����ԭ��ʱ�������ܵĻ�ѧ����ʽΪ____________________________��
��5�����ڹ�����I����������������Һ����������Ҫ��ߡ����о��߲��ù�����II����ð�.��������������У������ĵ缫��ӦʽΪ____________________________________��
��6����ҵ�����У�����2��������������Һ3������3��
����Һ3����Һ1�Ͼ�������ͭ���ϵͳ���ô�����ʩ���ŵ�Ϊ_____________________________��
������3������Auspan>��Ag������_____�����߷��롣(����ĸ)
A.��ˮ B.ϡ���� C.Ũ����������Һ D.Ũ����
����Ŀ���ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ�����
�� �ȣ��棩 | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1�������ϱ����ݿ�֪�÷�ӦΪ_____ ������ȣ����ȣ���ȷ��������Ӧ��
�����д�ʩ������������ԭ��������_____������ţ���
a������ѹǿ�����ںϳɰ� b��ʹ�ú��ʵĴ��������ڿ������ɰ�
c����������Ҫ�����¶���500��C���� d����Ҫʹ�ù�����N2�����H2ת����
��2��0.2mol��������ˮ�����뺬��0.2mol�������Һ��Ӧ����QkJ���������Ȼ�ѧ����ʽ��ʾ�䷴Ӧʽ_____��
��3������ʱ����amol��������ˮ����ͨ��bmol�Ȼ��⣬��Һ���Ϊ1L����c��NH4+��=c��Cl��������һˮ�ϰ��ĵ���ƽ�ⳣ��Kb=_____����ab��ʾ����
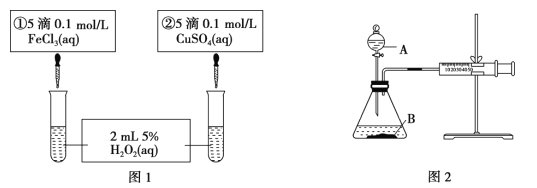
��4��ԭ����H2��ͨ����Ӧ CH4��g��+H2O ��g��![]() CO��g��+3H2��g�� ��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO��g��+3H2��g�� ��ȡ����֪�÷�Ӧ�У�����ʼ������е�![]() �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ����ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ����ͼ��ʾ��

��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ�ǣ�P1_____P2�����������=����������
����������һ���������¶ȣ������IJ��ʻ�__�����������С����С�������䡱���䣩��
��5��ԭ����H2����ͨ����ӦCO��g��+H2O��g��![]() CO2��g��+H2��g����ȡ��
CO2��g��+H2��g����ȡ��
��T��ʱ�����ݻ��̶�Ϊ5L�������г���1molˮ������1mol CO����Ӧ��ƽ����CO��Ũ��Ϊ0.08molL��1�����¶��·�Ӧ��ƽ�ⳣ��KֵΪ_____��
�ڱ����¶���ΪT�����ݻ����Ϊ5L���ı�ˮ������CO�ij�ʼ���ʵ���֮�ȣ������������з�Ӧ�����������ܹ�˵����ϵ����ƽ��״̬����_____������ţ���
a��������ѹǿ����ʱ��ı�
b�����������ܶȲ���ʱ��ı�
c����λʱ��������a mol CO2��ͬʱ����a mol H2
d���������n��CO����n��H2O����n��CO2����n��H2��=1��16��6��6