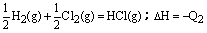题目内容
已知2 mol氢气完全燃烧生成水蒸气时放出能量484 kJ,且氧气中1 mol O=O键完全断裂时吸收能量496 kJ,水蒸气中1 mol H–O键形成时放出能量463 kJ,则氢气中1 mol H–H键断裂时吸收能量为
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
C
试题分析:反应热就是断键吸收的能量和形成化学键所放出的能量的差值,据此可知,2×2×463kJ-496kJ-2x=484kJ,解得x=436kJ,答案选C。
点评:该题是中等难度的试题,也是高考中的常见考点,试题基础性强,难度不大。该题的关键是明确反应热与化学键的关系,有助于培养学生的逻辑推理能力,提高学生学习兴趣和学习积极性。

练习册系列答案
相关题目
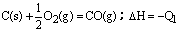 C(s) + O2(g)=CO2(g);△H=-Q2
C(s) + O2(g)=CO2(g);△H=-Q2