题目内容
下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②向100 mL0.1 mol/L 的溴化亚铁溶液中通入0.05 mol的氯气时发生反应的离子方程式:
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
③斜长石KAlSi3O8的氧化物形式可表示为:K2O?Al2O3?3SiO2
④酸性条件下KIO3溶液与KI溶液发生反应生成I2时的离子方程式:
IO3-+5I-+3H2O=I2+6OH-
⑤碳酸氢根离子的电离方程式可表示为: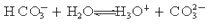
⑥元素周期表中,从上到下,卤族元素的非金属性逐渐减弱,氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放
热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 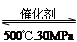 2NH3(g) △H=" -38.6" kJ·mol-1
2NH3(g) △H=" -38.6" kJ·mol-1
| A.全部 | B.②⑤ | C.②③④⑦ | D.②④⑦ |
B
解析试题分析:①中活性炭利用吸附性漂白物质(物理变化)、SO2与品红等发生化合反应生成无色不稳定的物质(非氧化还原反应),HClO具有强氧化性将有色物质氧化褪色(氧化还原反应),其漂白的化学原理不同,错误;③KAlSi3O8的氧化物形式应该表示为:K2O?Al2O3?6SiO2,错误;④由于反应在酸性条件下,其正确的离子方程式为IO3-+5I-+6H+=I2+3H2O;⑥卤族元素(从上到下)的氢卤酸的酸性依次增强,错误;⑦由于该反应为可逆反应,0.5 mol N2和1.5 mol H2不能完全反应,故其△H<-38.6 kJ·mol-1,错误。
考点: 考查物质的漂白原理、离子方程式的书写、电离方程式的书写、硅酸盐改写为氧化物形式、元素周期律(氢化物酸性)、可逆反应与反应热的计算等。

 阅读快车系列答案
阅读快车系列答案下列离子方程式中正确的是
A.Cl2通入水中:Cl2+H2O 2H++Cl-+C1O- 2H++Cl-+C1O- |
| B.钢铁发生吸氧腐蚀时,铁作负极:Fe-3e-=Fe3+ |
| C.向双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O |
D.用铜作阳极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2 2Cu+O2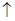 +4H+ +4H+ |
在水溶液中能大量共存的一组是
| A.Fe2+、Na+、ClO-、Cl- | B.Al3+、Mg2+、SO42-、CO32- |
| C.H+、Ca2+、Cl-、NO3- | D.AlO2-、Cl-、H+、K+ |
某无色透明溶液能与铝粉反应放出H2,则此溶液中一定能大量共存的离子组为
| A.OH-、Na+、K+、MnO4- | B.H+、Cl-、Ba2+、NO3- |
| C.K+、Cl-、Na+、SO42- | D.NH4+、Mg2+、Cl-、HCO3- |
下列反应的离子方程式正确的是( )
| A.向AgNO3溶液中滴加氨水至过量:Ag++NH3·H2O=AgOH↓+NH4+ |
| B.向Mg(OH)2悬浊液中滴加FeCl3溶液:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| C.向Na2S2O3溶液中加入足量稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O |
D.向苯酚钠溶液中通入少量CO2气体: |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1 mol/L的NaOH溶液:K+、AlO2-、SO42-、CO32- |
| B.0.1 mol/LFeCl3溶液:K+、NH4+、I-、SCN- |
| C.0.1 mol/L的Na2CO3溶液:K+、Ba2+、NO3-、Cl- |
| D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、I-、NO3- |
下列反应的离子方程式中,正确的是
| A.NH4HCO3溶液与过量NaOH溶液反应:NH4+ + OH- = NH3·H2O |
| B.在苯酚的乳浊溶液中滴加碳酸钠溶液变澄清:2C6H5OH + CO32- → CO2↑+ 2C6H5O- + H2O |
C.用两根铜棒作电极电解盐酸:2H+ + 2Cl-  H2↑ + Cl2↑ H2↑ + Cl2↑ |
| D.SO2通入次氯酸钠溶液中:SO2 + ClO-+ H2O = SO42- + Cl-+ 2H+ |
常温下,下列各组粒子在指定溶液中可能大量共存的是( )
| A.氨水中:Al3+、Cl-、I-、SO42- | B.pH=2的溶液中:K+、Cu2+、Cl-、NO3- |
| C.食盐水中:Mg2+、Fe(OH)2、Br-、CO32- | D.无色溶液:NO3-、SO2、NH4+、Na+ |
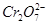 +H+—→CO2↑+Cr3++H2O,当这个方程式配平后,H+的化学计量数为
+H+—→CO2↑+Cr3++H2O,当这个方程式配平后,H+的化学计量数为