题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1 mol/L的NaOH溶液:K+、AlO2-、SO42-、CO32- |
| B.0.1 mol/LFeCl3溶液:K+、NH4+、I-、SCN- |
| C.0.1 mol/L的Na2CO3溶液:K+、Ba2+、NO3-、Cl- |
| D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、I-、NO3- |
A
解析试题分析:A、K+、AlO2-、SO42-、CO32-在碱性条件下不发生离子反应,可以大量共存,正确;B、SCN-、I-都可与Fe3+发生离子反应而不能大量共存,错误;C、Ba2+与CO32-结合生成碳酸钡沉淀,不能大量共存,错误;D、c(H+)/c(OH-)=1×1014的溶液中c(H+)=1mol/L,溶液为酸性溶液,酸性条件下I-、NO3-发生氧化还原反应而不能大量共存,错误,答案选A。
考点:考查离子的电离共存问题

练习册系列答案
相关题目
能正确表示下列反应的离子方程式是
| A.Cl2通入NaOH溶液:Cl2+OH-=Cl-+ClO-+H2O |
| B.NaHCO3溶液中加入稀HCl:CO32-+2H+=CO2↑+H2O |
| C.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| D.Cu溶于稀HNO3:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是
| A.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| C.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- |
| D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得 |
下列说法正确的是( )
| A.根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可检验绿矾(FeSO4·7H2O)是否变质 |
| B.根据反应H3PO3+2NaOH(足量)===Na2HPO3+2H2O可知:H3PO3属于三元酸 |
| C.根据反应3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O可知:反应中HNO3表现酸性和氧化性 |
| D.根据反应CuSO4+H2S===CuS↓+H2SO4可知:H2S的酸性比H2SO4强 |
下列各组离子在给定条件下能大量共存的是
| A.强酸性溶液中:NH4+、K+、ClO-、Cl- |
| B.有SO42—存在的溶液中:Na+、Mg2+、Ba2+、I- |
| C.加入铝粉能放出氢气的溶液中:K+、Ba2+、Cl-、Br- |
| D.在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+ |
能正确表示下列反应的离子方程式是( )
| A.硫酸铝溶液中加入过量氨水 Al3++3OH﹣=Al(OH)3↓ |
| B.碳酸钠溶液中加入澄清石灰水 Ca(OH)2+CO32﹣=CaCO3↓+2OH﹣ |
| C.冷的氢氧化钠溶液中通入氯气 Cl2+2OH﹣=ClO﹣+Cl﹣+H2O |
| D.稀硫酸中加入铁粉 2Fe+6H+=2Fe3++3H2↑ |
下列在指定溶液中的各组离子,能够大量共存的是
| A.使无色酚酞变红的溶液中:S2—、K+、CO32—、C1— |
| B.1mol·L—1的氯化铁溶液中:Na+、C1—、SCN—、Cu2+ |
| C.PH=0的溶液中:S2—、I—、Mg2+、Ba2+ |
| D.水电离的C(H+)=10—13mol·L—1的溶液中:Fe2+、SO42—、K+、NO3— |
在水溶液中能大量共存的一组离子是( )
| A.HCO3-、H+、NO3-、Na+ |
| B.Na+、Cu2+、OH-、SO42- |
| C.Mg2+、H+、AlO2-、SO42- |
| D.NH4+、K+、Br-、NO3- |
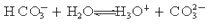
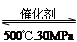 2NH3(g) △H=" -38.6" kJ·mol-1
2NH3(g) △H=" -38.6" kJ·mol-1