题目内容
17.一定温度下,在容积为2L的密闭容器中进行反应:aM(气)?bN(气).M、N的物质的量随时间的变化如图所示,下列表述中正确的是( )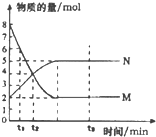
| A. | 反应式中a:b=2:5 | |
| B. | 0-t1物质M的浓度c(M)减少了1mol•L-1 | |
| C. | t2时,c(M)=c(N)=4mol•L-1,反应一定达到平衡状态 | |
| D. | t3时,c(M)不再变化,正反应速率小于逆反应速率 |
分析 A.根据图知,在反应中M的物质的量减少、N的物质的量增大,所以M是反应物、N是生成物,反应达到平衡状态时,△n(M)=(8-2)mol=6mol、△n(N)=(5-2)mol=3mol,同一时间段内各物质的物质的量变化量之比等于其计量数之比,所以M、N的计量数之比=6mol:3mol=2:1,所以反应方程式为2M(气)?N(气);
B.0-t1物质M的浓度c(M)减少了8−628−62mol•L-1;
C.t2时,c(M)=c(N)=2mol•L-1,该反应正逆反应速率不相等;
D.t3时,c(M)不再变化,该反应达到平衡状态.
解答 解:A.根据图知,在反应中M的物质的量减少、N的物质的量增大,所以M是反应物、N是生成物,反应达到平衡状态时,△n(M)=(8-2)mol=6mol、△n(N)=(5-2)mol=3mol,同一时间段内各物质的物质的量变化量之比等于其计量数之比,所以M、N的计量数之比=6mol:3mol=2:1,所以a:b=2:1,
故A错误;
B.0-t1物质M的浓度c(M)减少了8−628−62mol•L-1=1mol/L,故B正确;
C.t2时,c(M)=c(N)=2mol•L-1,根据图知,随着反应的进行,M的物质的量还在减少、N的物质的量还在增加,所以平衡向正反应方向移动,没有达到平衡状态,故C错误;
D.t3时,c(M)不再变化,该反应达到平衡状态,则正逆反应速率相等,故D错误;
故选B.
点评 本题考查图象分析,明确图象中曲线综合坐标含义及曲线变化趋势是解本题关键,注意:反应体系中各物质的物质的量浓度相等时该反应不一定到达平衡状态,易错选项是C.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
7.温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)═PCl3(g)+Cl2(g),经过一段时间后达到平衡.反应过程中测定的t/s-n(PCl3)/mol数据如图.下列说法正确的是( )

| A. | 反应在前50 s 的平均速率v(PCl3)=0.0032 mol•L-1•s-1 | |
| B. | 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20mol PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) | |
| C. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| D. | 相同温度下,起始时向容器中充入2.0 mol PCl3 和2.0mol Cl2,达到平衡时,PCl3 的转化率小于80% |
8.在一定条件下,将分別盛有熔融氯化钾、氯化镁、氧化铝的三个电解槽串联、通电、电解,一段时间后,得到钾、镁、铝的物质的量之比为( )
| A. | 1:2:3 | B. | 3:2:1 | C. | 6:3:1 | D. | 6:3:2 |
12.下列说法错误的是( )
| A. | 只要有化学键断裂的变化一定是化学变化 | |
| B. | 并不是所有化学反应的速率都与压强有关 | |
| C. | 可逆反应达到平衡后,正、逆反应速率相等但不为零 | |
| D. | 装有NO2和N2O4混合气的密闭烧瓶加热后,颜色变深,说明该化学平衡发生了移动 |
9.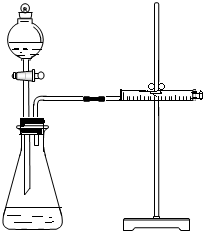 影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究.他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素.甲同学的实验报告如下表:
影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究.他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素.甲同学的实验报告如下表:
(1)甲同学表中实验步骤②为分别投入大小、形状相同的Al、Fe、Mg.
(2)甲同学的实验目的是探究探究反应物本身的性质对反应速率的影响.
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验.
(3)乙同学在实验中应该测定的数据是测定同一金属与浓度不同但体积相同的硫酸产生一定体积的气体所需要的时间于(或在一定时间内产生气体的体积).
(4)乙同学完成实验应选用的实验药品是Mg(或Fe)和 0.5mol/L、2mol/L的硫酸.
 影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究.他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素.甲同学的实验报告如下表:
影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究.他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素.甲同学的实验报告如下表:| 实验步骤 | 现象 | 结论 |
| ①分别取等体积2mol/L的硫酸于试管中 ② | Mg产生气泡速率快于Fe,Cu无明显变化 | 金属性质越活泼,反应速率越快 |
(2)甲同学的实验目的是探究探究反应物本身的性质对反应速率的影响.
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验.
(3)乙同学在实验中应该测定的数据是测定同一金属与浓度不同但体积相同的硫酸产生一定体积的气体所需要的时间于(或在一定时间内产生气体的体积).
(4)乙同学完成实验应选用的实验药品是Mg(或Fe)和 0.5mol/L、2mol/L的硫酸.
6.下列有关判断正确的是( )
| A. | 反应C(s)+CO2(g)═2CO(g)的△H>0,△S<0 | |
| B. | 反应H+(aq)+OH-(aq)═H2O(l)的△H<0,△S<0 | |
| C. | 反应NH3(g)+HCl(g)═NH4Cl(s) 在低温下能自发进行,则该反应△H>0 | |
| D. | 反应CaCO3(s)═CaO(s)+CO2(g) 室温下不能自发进行,则该反应△H<0 |
7.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | |
| B. | 金刚石、石墨和“足球稀”C60为同素异形体 | |
| C. | 碳链为 与 与 的烃为同系物 的烃为同系物 | |
| D. |  和 和 互为同分异构体 互为同分异构体 |