题目内容
【题目】氢卤酸能量关系如图。下列说法不正确的是:
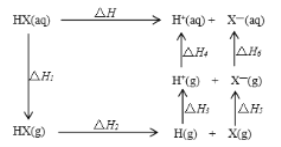
A. 相同条件下,HCl的△H2比HBr的小
B. 已知HF气体溶于水放热,则HF的△H1>0
C. 相同条件下,HCl的△H3+△H4与HI的一样大
D. 一定条件下气态原子生成1 mol H-X键放出a kJ能量,则该条件下△H2=a kJ mol-1
【答案】A
【解析】
A.由氢卤酸能量关系图知,△H2是气态卤化氢断裂化学键生成气态原子过程的焓变,断裂化学键需要吸收能量即△H2>0,因为卤素(X)的非金属性越强,H-X键就越强,断裂需要的吸收的能量就越多,因非金属性Cl>Br,所以H-Cl键断裂吸收的能量比H-Br键断裂吸收的能量多,所以相同条件下,HCl的△H2比HBr的大,A项错误;
B.HF气体溶于水的过程分两步:HF(g)=HF(aq),-△H1;HF(aq)=H+(aq)+F-(aq), △H。两热化学方程式相加得总过程热化学方程式为:HF(g)=H+(aq)+F-(aq),-△H1+△H <0,即△H1>△H,因电离过程吸收热量即△H>0,所以△H1>0,B项正确;
C.HCl气体和HI气体溶于水的过程都存在:气态氢原子失电子形成气态氢离子,气态氢离子溶于水形成水合氢离子的过程,该过程的总焓变为△H3+△H4,所以相同条件下HCl的△H3+△H4与HI的一样大,C项正确;
D.根据一定条件下气态原子生成1 mol H-X键放出a kJ能量,有热化学方程式:H(g)+X(g)= HX(g), △H=-akJ/mol。由氢卤酸能量关系图知HX(g)=H(g)+X(g),△H2,则△H2=+a kJ/mol,D项正确;答案选A。

【题目】游离态氮称为惰性氮,游离态氮转化为化合态氮称之为氮的活化,在氮的循环系统中,氮的过量“活化”,则活化氮开始向大气和水体过量迁移,氮的循环平衡被打破,导致全球环境问题。
Ⅰ. 氮的活化
工业合成氨是氮的活化重要途径之一,在一定条件下,将N2 和 H2 通入到体积为0.5L的恒容容器中,反应过程中各物质的物质的量变化如图所示:

(1)10min内用NH3表示该反应的平均速率,v(NH3)=____________。
(2)在第10min和第25min改变的条件可能分别是_________、________(填字母)。
A.加了催化剂 B. 升高温度 C. 增加NH3的物质的量
D.压缩体积 E.分离出氨气
(3)下列说法能说明该可逆反应达到平衡状态的是__________(填字母)。
A. 容器中气体密度不变 B. 容器中压强不变
C. 3v(H2)正=2v(NH3)逆 D. N2、H2、NH3分子数之比为1∶3∶2
Ⅱ.催化转化为惰性氮 已知:SO2、CO、NH3等都可以催化还原氮氧化物生成惰性氮。
(4)在250C、101KPa时,N2(g)+3H2(g) ![]() 2NH3(g) △H1= -92.4kJ/mol.
2NH3(g) △H1= -92.4kJ/mol.
2H2(g)+O2(g)=2H2O(l) △H2= -571.6 kJ/mol
N2(g)+O2(g)=2NO(g) △H3= +180kJ/mol
则NO与NH3反应生成惰性氮的热化学方程式______________________________。
(5)在有氧条件下,新型催化剂M能催化CO与NOx反应生成N2。现向某密闭容器中充入等物质的量浓度的NO2和CO气体,维持恒温恒容,在催化剂作用下发生反应:
4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) △H<0,相关数据如下:
N2(g)+4CO2(g) △H<0,相关数据如下:
0min | 5min | 10min | 15min | 20min | |
c(NO2) /mol·L-1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
c(N2) /mol·L-1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①计算此温度下的化学平衡常数K=______,
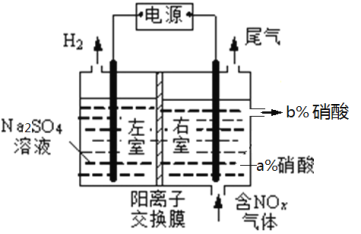
②实验室模拟电解法吸收NOx装置如图,(图中电极均为石墨电极)。若用NO2气体进行模拟电解法吸收实验(a<b),电解时NO2发生反应的电极反应式:_________________________________。