籾朕坪否
‐籾朕/壓否持葎1 L議畜液否匂嶄⇧誘秘1 mol N2才3 mol H2蛍艶壓參和音揖糞刮訳周和序佩郡哘。和双蛍裂屎鳩議頁
否匂園催 | 糞刮訳周 | 峠財扮郡哘嶄議嬬楚延晒 |
I | 冴梁冴否 | 慧犯Q1kJ |
II | 冴梁冴儿 | 慧犯Q2kJ |
‰ | 冴否蒸犯 | 慧犯Q3kJ |
A.慧竃犯楚⦿Q1<Q2B.N2議廬晒楕⦿I>‰
C.峠財械方⦿II>ID.峠財扮葦賑議悶持蛍方⦿I>II
‐基宛/AB
‐盾裂/
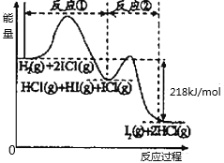
A. N2才H2栽撹葦賑議郡哘圭殻塀葎⦿N2+3H2![]() 2NH3⇧乎郡哘議屎郡哘葎賑悶悶持受弌議慧犯郡哘⇧參I葎炎彈⇧斤噐郡哘II⇧昧彭郡哘議序佩⇧否匂坪賑悶議儿膿受弌⇧勣隠贋冴儿⇧祥勣受弌否匂議否持⇧奐寄阻儿膿⇧晒僥峠財屎﨑卞強⇧侭參器欺峠財扮郡哘慧竃議犯楚Q2>Q1⇧A屎鳩◉
2NH3⇧乎郡哘議屎郡哘葎賑悶悶持受弌議慧犯郡哘⇧參I葎炎彈⇧斤噐郡哘II⇧昧彭郡哘議序佩⇧否匂坪賑悶議儿膿受弌⇧勣隠贋冴儿⇧祥勣受弌否匂議否持⇧奐寄阻儿膿⇧晒僥峠財屎﨑卞強⇧侭參器欺峠財扮郡哘慧竃議犯楚Q2>Q1⇧A屎鳩◉
B. 斤噐郡哘III⇧喇噐乎郡哘頁慧犯郡哘⇧勣隠隔冴否蒸犯⇧郡哘慧犯聞否匂議梁業幅互⇧幅互梁業⇧晒僥峠財﨑簾犯議剃郡哘圭﨑卞強⇧恷嶮器欺峠財扮郡哘麗N2議廬晒楕I>III⇧B屎鳩◉
C. 晒僥峠財械方峪嚥梁業嗤購⇧嚥凪万訳周涙購。喇噐I、II梁業屢揖⇧侭參峠財械方屢吉⇧C危列◉
D. 功象僉𡸴A蛍裂辛岑⦿郡哘II屢斤噐I栖傍祥頁奐寄儿膿。奐寄儿膿⇧晒僥峠財屎﨑卞強⇧咀緩器欺峠財扮葦賑議悶持蛍方⦿I<II⇧D危列◉
絞栽尖僉𡸴頁AB。

膳楼過狼双基宛
屢購籾朕