题目内容
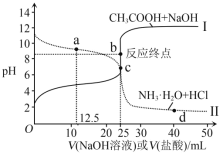
【题目】室温下向10mL0.1mol·L-1NaOH溶液中加入0.1mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )

A.b点所示溶液中[A-]>[HA]
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,[Na+]=[A-]+[HA]
D.a点所示溶液中[Na+]>[A-]>[H+]>[HA]
【答案】A
【解析】
A、b 点溶液中溶质为等物质的量NaA和HA ,溶液呈酸性,说明HA的电离程度大于NaA的水解程度,所以c(A-)> c((HA),选项A正确;
B、a 点NaA发生了水解反应,促进了水的电离,b点主要由于HA的电离而使溶液呈酸性,抑制了水的电离,所以a点水的电离程度大于b点,选项B错误;
C、根据电荷守恒: c(Na+)+c (H+)=c (A-)+c (OH-),pH=7,则c (H+)=c (OH-),可得 c (Na+)=c (A-),选项C错误;
D、a 点NaOH与HA 恰好完全反应,溶液的 pH为8.7,呈碱性,说明HA为弱酸,NaA发生了水解反应,则溶液中 c (Na+)> c (A-)> c (OH-)> c (HA)> c (H+) ,选项D错误;
答案选A。

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目