题目内容
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展做出巨大贡献的科学家,锂离子电池广泛应用于手机、笔记本电脑等。
(1)锂元素在元素周期表中的位置:_________________。
(2)氧化锂(Li2O)是制备锂离子电池的重要原料,氧化锂的电子式为_____________。
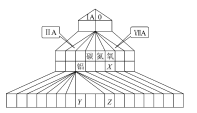
(3)近日华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出了石墨烯电池,电池反应式为LIxC6+Li1-x![]() C6+LiCoO2,其工作原理如图。
C6+LiCoO2,其工作原理如图。

①石墨烯的优点是提高电池的能量密度,石墨烯为层状结构,层与层之间存在的作用力是_______。
②锂离子电池不能用水溶液做离子导体的原因是___________(用离子方程式表示)。
③锂离子电池放电时正极的电极反应式为________________。
④请指出使用锂离子电池的注意问题____________________。(回答一条即可)
【答案】第二周期第IA族 ![]() 范德华力(分子间作用力) 2Li+2H2O=2Li++2OH-+H2↑ Li1-xCoO2+xLi++xe-= LiCoO2 避免过充、过放、过电流、短路及热冲击或使用保护元件等
范德华力(分子间作用力) 2Li+2H2O=2Li++2OH-+H2↑ Li1-xCoO2+xLi++xe-= LiCoO2 避免过充、过放、过电流、短路及热冲击或使用保护元件等
【解析】
(1)根据锂元素的原子结构与元素位置的关系分析判断;
(2)氧化锂是离子化合物,Li+与O2-之间通过离子键结合;
(3)①石墨烯结构是平面结构,层内是共价键,层间以分子间作用力结合;
②根据Li是碱金属元素,利用碱金属单质的性质分析;
③锂离子电池放电时正极上Li+得电子变为LiCoO2;
④使用锂离子电池的注意问题是禁止过充、过房,配备相应的保护元件等。
(1)Li是3号元素,核外电子排布为2、1,所以Li在元素周期表的位置位于第二周期第IA族;
(2) Li2O是离子化合物,Li+与O2-之间通过离子键结合,其电子式为:![]() ;
;
(3)①石墨烯的优点是提高电池的能量密度,石墨烯为层状结构,在层内,C原子之间以共价键结合,在层与层之间存在的作用力是分子间作用力,也叫范德华力;
②Li是碱金属元素,单质比较活泼,容易和水反应产生氢气,反应方程式为:2Li+2H2O=2Li++2OH-+H2↑,所以锂离子电池不能用水溶液;
③根据锂电池总反应方程式可知:锂离子电池在放电时,正极上Li+得电子变为LiCoO2,电极反应式为:Li1-xCoO2+xLi++xe-= LiCoO2;
④锂电池在使用时应该注意的问题是避免过充、过放、过电流、短路及热冲击或使用保护元件等。

【题目】在容积为1 L的密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应。下列分析正确的是
容器编号 | 实验条件 | 平衡时反应中的能量变化 |
I | 恒温恒容 | 放热Q1kJ |
II | 恒温恒压 | 放热Q2kJ |
Ⅲ | 恒容绝热 | 放热Q3kJ |
A.放出热量:Q1<Q2B.N2的转化率:I>Ⅲ
C.平衡常数:II>ID.平衡时氨气的体积分数:I>II