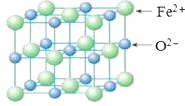
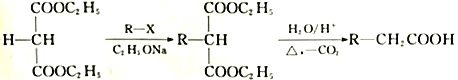题目内容
【题目】常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3(红褐色固体)。
(1)Fe(OH)3中铁元素化合价为______,该脱氧反应中还原剂是_________。
(2)某化学兴趣小组用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g氯化钠)进行如下两个实验。
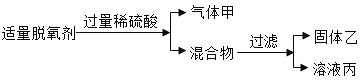
请回答:
①溶液丙中一定含有的金属阳离子是_________(写离子符号);
②检验溶液丙中Cl的方法是_____________________________________________。
将乙烘干后进行如下实验,物质之间的转化关系如图(部分产物略去)
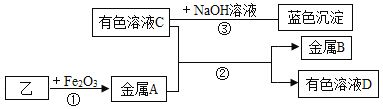
③写出反应②的离子方程式,并用双线桥法表示电子转移的方向和数目_________;
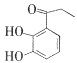
④向溶液C中加入BaCl2溶液,有白色沉淀产生,其离子方程式为____________;反应③的化学方程式为______________________________。
【答案】+3 Fe(OH)2 Fe2+、Na+ 取少许溶液丙于试管中,向试管中加入过量的Ba(NO3)2溶液,振荡,静置,向上层清液中滴加AgNO3溶液,观察到有白色沉淀产生,溶液丙中含有Cl 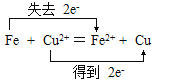 SO42 + Ba2+ =BaSO4↓ CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4
SO42 + Ba2+ =BaSO4↓ CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4
【解析】
(1)Fe(OH)3中铁元素化合价为+3价,脱氧反应中4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3中Fe(OH)2的化合价由+2→+3,化合价升高,作还原剂,故答案为:+3,Fe(OH)2;
(2)①脱氧剂中铁和硫酸反应生成硫酸亚铁和氢气,气体甲是氢气,反应后的混合物中有硫酸、硫酸亚铁、食盐、活性炭,过滤除去了活性炭,溶液丙中含有的溶质是硫酸、硫酸亚铁、氯化钠,含有的金属阳离子是Fe2+、Na+,故答案为:Fe2+、Na+;
②检验溶液中Cl的方法是取少许溶液丙于试管中,向试管中加入过量的Ba(NO3)2溶液,振荡,静置,向上层清液中滴加AgNO3溶液,观察到有白色沉淀产生,溶液丙中含有Cl,故答案为:少许溶液丙于试管中,向试管中加入过量的Ba(NO3)2溶液,振荡,静置,向上层清液中滴加AgNO3溶液,观察到有白色沉淀产生,溶液丙中含有Cl;
③由物质之间的转化关系可知,固体乙的主要成分是碳,在高温条件下碳与氧化铁反应生成了铁,能与氢氧化钠反应生成蓝色沉淀的溶液是硫酸铜溶液,所以有色溶液C是硫酸铜,铁与硫酸铜反应生成铜和硫酸亚铁。所以反应②的离子方程式为Cu2++Fe=Fe2++Cu,Cu2+→Cu,得到2个电子,Fe→Fe2+失去2个电子,用双线桥法表示电子转移的方向和数目为: ,故答案为:
,故答案为: 。
。
④由③分析可知有色溶液C是硫酸铜,向CuSO4溶液中加入BaCl2溶液,有白色沉淀产生,白色沉淀为硫酸钡沉淀,其离子方程式为SO42 + Ba2+ =BaSO4↓,硫酸铜与氢氧化钠反应的化学方程式为:CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4,故答案为:SO42 + Ba2+ =BaSO4↓, CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4。