题目内容
14.晶体硅是一种重要的非金属材料,工业上用碳在高温下还原石英砂(主要成份为含铁、铝等杂质的二氧化硅)得粗硅,粗硅与氛气在450-500℃条件下反应生成四氯化硅,四氯化硅经提纯后与过量H2在1100℃-1200℃条件下反应制得高纯硅.以下是实验室制备SiCl4的装置示意图.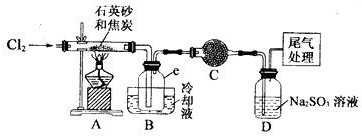
实验过程中,石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl4,A1C13,FeCl3遇水均易水解,有关物质的物理常数见下表:
| 物质 | SiC14 | A1C13 | FeC13 |
| 沸点/℃ | 57.7 | - | 315 |
| 熔点/℃ | -70.0 | - | - |
| 升华温度/℃ | - | 180 | 300 |
(1)实验室制备氯气有以下五步操作,其正确操作顺序为④③⑤②①(填标号).
①向烧瓶中装入二氧化锰固体,向分液漏斗中加入浓盐酸
②检查装置的气密性
③把酒精灯放在铁架台上,根据酒精灯火焰确定铁圈高度,固定铁圈,放上石棉
④在烧瓶上装好分液漏斗,安装好导气管
⑤将烧瓶固定在铁架台上
(2)装置A的硬质玻璃管中发生主要反应的化方程式是2C+SiO2+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4+2CO↑.装置A.B间导管短且粗的原因是防止生成物中的AlCl3、FeCl3等杂质凝结成固体堵塞导管;验中尾气处理的方法是连接一个加热的装有CuO粉末的反应管.
(3)装置B中e瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氛化硅.在精馏过程中,不可能用到的仪器有CD(填正确答案标号).
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(4)装置D中的Na2SO3的作用主要是吸收未反应完的Cl2请设计一个实验,证明装置D中的Na2SO3已被氧化(简述实验步骤):取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化.
(5)SiCl4极易水解,其完全水解的产物为H4SiO4(或H2SiO3)和HCl.H2还原SiCl4制得高纯硅的过程中若混入O2,可能引起的后果是可能引起爆炸;硅被氧化得不到高纯硅.
分析 A中发生二氧化硅和碳和氯气反应生成四氯化硅,由信息可知,四氯化硅的沸点低,则B装置冷却可收集四氯化硅,C可防止防止B右端的水蒸气进入B与四氯化硅反应,造成产物不纯,最后D处理含氯气的尾气.
(1)在实验室中由浓盐酸和二氧化锰制备氯气,按照先下后上,先左后右的原则搭建实验装置,因制备气体,所以需检查装置的气密性,然后装入药品进行制备;
(2)在D装置中二氧化硅和碳和氯气反应生成四氯化硅和一氧化碳;产物中有AlCl3、FeCl3防止凝结成固体堵塞导管,尾气主要为一氧化碳,可用氧化铜检验;
(3)根据精馏(类似多次蒸馏)原理,精馏过程中不可能用到吸滤瓶和球形冷凝器管;
(4)氯气有强氧化性,亚硫酸根离子有还原性,所以氯气和亚硫酸根离子能发生氧化还原反应生成硫酸根离子、氯离子和氢离子;如果亚硫酸钠被氧化会生成硫酸钠,根据硫酸根离子的检验方法检验即可;
(5)SiCl4极易水解,生成原硅酸和氯化氢,氢气和氧气混合在加热的条件下易发生爆炸,硅易与氧气反应生成氧化硅.
解答 解:(1)加热条件下,实验室用浓盐酸和二氧化锰制取氯气,二者反应生成氯化锰、氯气和水,方程式为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,搭建实验装置应先下后上,先左后右的原则,所以先在烧瓶上装好分液漏斗,安装好导气管,把酒精灯放在铁架台上,根据酒精灯火焰确定铁圈高度,固定铁圈,放上石棉,将烧瓶固定在铁架台上,因制备气体,所以需检查装置的气密性,然后装入药品,所以检查装置的气密性,向烧瓶中装入二氧化锰固体,向分液漏斗中加入浓盐酸,即正确操作顺序为④③⑤②①,
故答案为:③⑤②①;
(2)在A装置中二氧化硅和碳和氯气反应生成四氯化硅和一氧化碳,反应为:2C+SiO2+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4+2CO↑,生成物中有AlCl3、FeCl3等杂质,凝结成固体堵塞导管,所以装置A.B间导管短且粗,尾气主要为一氧化碳,氧化铜和一氧化碳在加热的条件下反应生成二氧化碳和铜,铜为红色固体,所以可用氧化铜验尾气,
故答案为:2C+SiO2+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4+2CO↑;防止生成物中的AlCl3、FeCl3等杂质凝结成固体堵塞导管;连接一个加热的装有CuO粉末的反应管;
(3)吸滤瓶用于减压过滤装置中,与精馏(类似多次蒸馏)无关,球形冷凝管含有球形部分区域,不适合精馏,蒸馏需圆底烧瓶盛放待蒸馏的液体,需温度计测量蒸气的温度,需接收器接受馏分,
故答案为:CD;
(4)亚硫酸钠被氧化生成硫酸钠,只有验证硫酸根离子的存在就可证明亚硫酸钠已经被氧化,检验硫酸根离子的存在选用试剂稀盐酸和氯化钡溶液,实验设计如下:取少量溶液置于洁净试管中,向其中加入稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,证明Na2SO3已被氧化,
故答案为:取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体;再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化;
(5)SiCl4水解反应方程式为:SiCl4+4H2O═H4SiO4↓+4HCl↑,生成原硅酸氯化氢,原硅酸易失去水生成硅酸H2SiO3,H2还原SiCl4制得高纯硅的过程中若混入O2,可能引起爆炸,硅被氧化得不到高纯硅,
故答案为:H4SiO4(或H2SiO3)和HCl;可能引起爆炸;硅被氧化得不到高纯硅.
点评 本题考查制备实验方案的设计,综合了氯气的制法、硅的提纯、SiCl4的制备等实验知识,注意把握制备原理及实验流程中的反应、物质的性质等为解答的关键,侧重分析与实验能力的综合考查,题目难度中等.

| A. | C22-的电子式是[ ]2- ]2- | |
| B. | Mg2C3和Li2C2与水反应生成的烃可能具有相同的官能团 | |
| C. | 1mol ZnC2与水反应生成的烃的体积约为22.4L | |
| D. | Al4C3与水反应生成的烃分子中只有极性键 |
| A. | Cl2+2NaOH═NaCl+NaClO+H2O | B. | Cl2+H2O═HCl+HClO | ||
| C. | Cl2+Cu$\frac{\underline{\;点燃\;}}{\;}$CuCl2 | D. | Cl2+H2$\frac{\underline{\;点燃\;}}{\;}$2HCl |
(1)写出该反应的平衡常数表达式$\frac{[N{H}_{3}]^{2}}{[{N}_{2}]×[{H}_{2}]^{3}}$,KA等于KB(选填“大于”、“小于”或“等于”).
(2)欲增大该反应K值,可以采取的措施为B
A 升高温度 B 降低温度 C 增大N2、H2的浓度 D 使用高效的催化剂
(3)分析以下表中数据后,完成下列问题[M(平)表示平衡时混合物的平均相对分子质量]
| 容器A | 容器B | |
| M(平) | 16.7 | |
| 平衡时N2的转化率 | 20% |
(4)常温下将氨气溶于水配成0.1mol/L的氨水100mL,此时溶液中$\frac{[{H}^{+}]}{[O{H}^{-}]}$=10-8,则溶液中NH3•H2O的电离程度用电离度表示为1%,水电离出的c(OH-)=10-11mol/L,再向溶液中加水稀释到1L,所得溶液中$\frac{[{H}^{+}]}{[O{H}^{-}]}$增大(填“增大、不变、减小或不确定”)
(5)已知三种酸的电离平衡常数如下表,浓度均为0.1mol/L的NaCN溶液、Na2CO3溶液、NaHCO3溶液和CH3COONa溶液的pH值分别为a、b、c、d,则a、b、c、d按从大到小的顺序排列为b>a>c>d,写出向NaCN溶液中通入少量CO2气体的离子方程式为CN-+CO2+H2O=HCN+HCO3-.
| 化学式 | 电离常数(298K) |
| 氢氰酸 | K=4.5×10-10 |
| 碳酸 | K1=4.4×10-7 K2=4.7×10-11 |
| 醋酸 | K=1.75×10-5 |
| A. | 1.4 g | B. | 2.2 g | C. | 4.4 g | D. | 在2.2~4.4 g之间 |
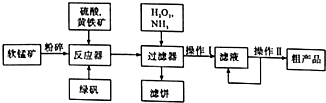 硫酸锰可作为饲料添加剂用于增肥,也可用于某些化学反应的催化剂,易溶于水,不溶于乙醇.工业上常用软锰矿(主要成分为MnO2,含有MgSO4等杂质)制备硫酸锰,其简化流程如下:
硫酸锰可作为饲料添加剂用于增肥,也可用于某些化学反应的催化剂,易溶于水,不溶于乙醇.工业上常用软锰矿(主要成分为MnO2,含有MgSO4等杂质)制备硫酸锰,其简化流程如下: