题目内容
【题目】某课题组为了深入探究二氧化硫的性质设计以下装置进行了实验。
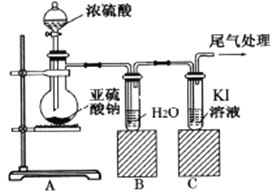
步骤一:检验装置气密性后向B、C中各加入20mL图示液体。
步骤二 :打开A中活塞,反应进行10分钟后关闭活塞。
步骤三:用pH计分别测量B、C 试管中溶液的pH。
结合上述实验,回答以下问题:
(1) 甲同学认为两瓶中pH大致相等,原因是二氧化硫溶于水后生成了酸性物质。该物质发生电离,其电离方程式为___________。
(2) 乙同学认为C瓶中pH可能更小,因为C中二氧化硫会像氧化硫化氢一样与碘离子发生氧化还原反应。通过pH计测定,B瓶中pH为2.13,C瓶中pH为1.05。为了解释该实验现象,该同学提出进行多次平行实验,目的是____________。测定结果如下:
第1次实验 | 第2次实验 | 第3 次实验 | |
B 瓶中pH | 2.15 | 2.10 | 2. 17 |
C 瓶中pH | 1.10 | 1.12 | 1.09 |
实验发现: C瓶中溶液的酸性始终比B瓶中的酸性强。
(3) 通过仔细观察,C瓶中溶液从无色变成浅黄色同时出现黄色浑浊,继续通入气体溶液又逐渐变为无色。其中溶液变黄且出现浑浊的过程对应的离子方程式为________,为了检验产物,中间取出少许溶液加入______,溶液变蓝,证明乙同学判断正确;黄色溶液又逐渐变为无色对应的化学反应方程式为_______________。
(4) 最终结论:
①B瓶中溶液呈弱酸性是由于__________。
②C瓶中溶液呈强酸性是由于生成了_________,该过程中体现出二氧化硫哪些化学性质_____。
【答案】 H2SO3![]() H++HSO3-, HSO3-
H++HSO3-, HSO3-![]() H++SO32- 减小实验误差 SO2+4I-+4H+=S↓+2I2+2H2O 淀粉溶液 SO2+I2+2H2O=H2SO4+2HI 亚硫酸部分电离产生了H+ 硫酸 氧化性和还原性
H++SO32- 减小实验误差 SO2+4I-+4H+=S↓+2I2+2H2O 淀粉溶液 SO2+I2+2H2O=H2SO4+2HI 亚硫酸部分电离产生了H+ 硫酸 氧化性和还原性
【解析】试题分析:(1) 二氧化硫溶于水后生成了亚硫酸,亚硫酸是二元弱酸;(2)进行多次平行实验,目的是进行对比,减小误差;(3) C瓶中溶液从无色变成浅黄色同时出现黄色浑浊,说明二氧化硫与碘离子反应生成碘单质和硫单质;碘能使淀粉变蓝;黄色溶液又逐渐变为无色,说明碘单质被二氧化硫还原为碘离子;(4)B中生成的是亚硫酸,C中生成的是硫酸;二氧化硫生成硫单质,硫元素化合价降低被还原,二氧化硫生成硫酸,硫元素化合价升高被氧化;
解析:(1) 二氧化硫溶于水后生成了亚硫酸,亚硫酸是二元弱酸,电离方程式是H2SO3![]() H++HSO3-, HSO3-
H++HSO3-, HSO3-![]() H++SO32-;(2)进行多次平行实验,目的是减小误差;(3) C瓶中溶液从无色变成浅黄色同时出现黄色浑浊,说明二氧化硫与碘离子反应生成碘单质和硫单质,反应的离子方程式是SO2+4I-+4H+=S↓+2I2+2H2O;碘能使淀粉变蓝,为了检验产物,取出少许溶液加入淀粉溶液,溶液变蓝,证明乙同学判断正确;黄色溶液又逐渐变为无色,说明碘单质被二氧化硫还原为碘离子,化学反应方程式为O2+I2+2H2O=H2SO4+2HI;(4) ①B中生成的是亚硫酸,亚硫酸部分电离产生了H+,所以B瓶中溶液呈弱酸性;C中生成的是硫酸,所以C瓶中溶液呈强酸性;二氧化硫生成硫单质,硫元素化合价降低被还原,二氧化硫生成硫酸,硫元素化合价升高被氧化,体现二氧化硫的氧化性和还原性;
H++SO32-;(2)进行多次平行实验,目的是减小误差;(3) C瓶中溶液从无色变成浅黄色同时出现黄色浑浊,说明二氧化硫与碘离子反应生成碘单质和硫单质,反应的离子方程式是SO2+4I-+4H+=S↓+2I2+2H2O;碘能使淀粉变蓝,为了检验产物,取出少许溶液加入淀粉溶液,溶液变蓝,证明乙同学判断正确;黄色溶液又逐渐变为无色,说明碘单质被二氧化硫还原为碘离子,化学反应方程式为O2+I2+2H2O=H2SO4+2HI;(4) ①B中生成的是亚硫酸,亚硫酸部分电离产生了H+,所以B瓶中溶液呈弱酸性;C中生成的是硫酸,所以C瓶中溶液呈强酸性;二氧化硫生成硫单质,硫元素化合价降低被还原,二氧化硫生成硫酸,硫元素化合价升高被氧化,体现二氧化硫的氧化性和还原性;

 阅读快车系列答案
阅读快车系列答案【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
实验编号 | HA物质的量浓度 | NaOH物质的量浓度 | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸 .
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2(选填“是”或“否”).混合液中离子浓度c(A﹣)与 c(Na+)的大小关系是 .
(3)丙组实验结果分析,HA是酸(选填“强”或“弱”).该混合溶液中离子浓度由大到小的顺序是 .
(4)丁组实验所得混合溶液中由水电离出的c(OH﹣)=molL﹣1 . 写出该混合溶液中下列算式的精确结果(不需做近似计算).c(Na+)﹣c(A﹣)=molL﹣1 c(OH﹣)﹣c(HA)=molL﹣1 .