题目内容
(1)请在下图所示分子的结构简式中用“*”标记出手性碳原子。若用该有机物进行核磁共振实验,所得核磁共振氢谱有________个峰,强度比为________。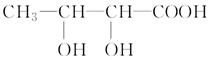
(2)已知某硼烷相对分子质量为28,核磁共振氢谱有两个峰且强度比为1∶2,则该硼烷的分子式是________,已知该硼烷气体在空气中能剧烈燃烧生成三氧化二硼和水,且生成1 mol液态水可放出722 kJ的热量,请写出燃烧的热化学方程式:____________________________。
(1)  6 3∶1∶1∶1∶1∶1
6 3∶1∶1∶1∶1∶1
(2)B2H62B2H6(g)+6O2(g) 2B2O3(s)+6H2O(l) ΔH=-4 332 kJ·mol-1
2B2O3(s)+6H2O(l) ΔH=-4 332 kJ·mol-1
解析试题分析:(1)手性碳原子所连的四个基团都是不同的,故该分子中共有2个手性碳原子,即 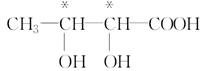 ,该分子中共有6类氢原子,且个数比为3∶1∶1∶1∶1∶1。(2)硼烷中只含有B和H两种元素,由于峰的强度比为1∶2,故分子中的氢原子数为3的倍数,故相对分子质量为28的硼烷的分子式为B2H6,1 mol B2H6燃烧生成3 mol H2O,故热化学方程式为2B2H6(g)+6O2(g)
,该分子中共有6类氢原子,且个数比为3∶1∶1∶1∶1∶1。(2)硼烷中只含有B和H两种元素,由于峰的强度比为1∶2,故分子中的氢原子数为3的倍数,故相对分子质量为28的硼烷的分子式为B2H6,1 mol B2H6燃烧生成3 mol H2O,故热化学方程式为2B2H6(g)+6O2(g) 2B2O3(s)+6H2O(l) ΔH=-4 332 kJ·mol-1。
2B2O3(s)+6H2O(l) ΔH=-4 332 kJ·mol-1。
考点:考查氢的种类和有机反应热化学方程式的书写。

 特高级教师点拨系列答案
特高级教师点拨系列答案I.已知:反应H2(g) + Cl2(g) = 2HCl(g) ΔH=" —184" kJ/mol
4HCl(g)+O2(g) 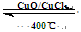 2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol
2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol 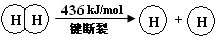

请回答:
(1)H2与O2反应生成气态水的热化学方程式
(2)断开1 mol H—O 键所需能量约为 kJ
II.试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: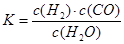 ,它所对应的化学方程式为:
,它所对应的化学方程式为:
(2)已知在400℃时,N2 (g)+ 3H2(g) 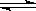 2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)
2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)
欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是 (填序号)(1分)
A.缩小体积增大压强 B.升高温度 C.加催化剂 D.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:A(g) + 3B(g) 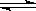 2C(g) + D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
2C(g) + D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
| t/K | 300 | 400 | 500 | … |
| K/(mol·L—1)2 | 4×106 | 8×107 | K1 | … |
请完成下列问题:
①判断该反应的ΔH 0(填“>”或“<”) (1分)
②在一定条件下,能判断该反应一定达化学平衡状态的是 (填序号)
A.3v(B)(正)=2v(C)(逆) B.A和B的转化率相等
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)以天然气(假设杂质不参与反应)为原料的燃料电池示意图如图所示。
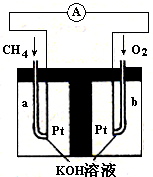
①放电时,负极的电极反应式为
②假设装置中盛装100.0 mL 3.0 mol·L—1 KOH溶液,放电时参与反应的氧气在标准状况下体积为8 960 mL。放电完毕后,电解质溶液中各离子浓度的大小关系为
已知:①溶液中CrO42—显黄色,Cr2O72-显橙红色
②PbCrO4难溶于水,也难溶于强酸
③H+(aq)+OH-(aq)=H2O(l); ΔH=" —a" KJ/mol
3Cl2(g)+2Cr3+(aq)+16OH-(aq)=2CrO42-(aq)+6Cl-(aq)+8H2O(l);ΔH="—b" KJ/mol
2CrO42-(aq)+2H+(aq)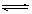 Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
平衡常数K=9.5×104 (上述a、b、c均大于0)
对上述反应⑤,取50mL溶液进行试验,部分测定数据如下:
| 时间(s) | 0 | 0.01 | 0.02 | 0.03 | 0.04 |
| n (CrO42—)(mol) | 0.01 | 8.0×10-4 | 5.4×10-4 | 5.0×10-4 | |
| n (Cr2O72—)(mol) | 0 | | 4.73×10-3 | | 4.75×10-3 |
试回答下列问题:
(1)0.02s到0.03s之间用Cr2O72-表示该反应的平均反应速率为
下列说法正确的( )
A、0.03s时V正(CrO42—)=2V逆(Cr2O72—)
B、溶液pH值不变说明该反应已达平衡状态
C、溶液中c(CrO42—):c(Cr2O72—)=2:1时该反应已达平衡状态
D、反应放热2.5×10-3c KJ时CrO42—的转化率为50%
E、升温该反应平衡常数变大
F、0.04s时加入足量的Pb(NO3)2 可使溶液由橙色变为黄色
(3)0.03s时溶液的pH=
(4)已知酸性条件下Cr2O72—将Cl-氧化为Cl2,本身被还原为Cr3+为放热反应,试写出该反应的热化学方程式:
氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱的原料,也是一种常用的制冷剂。
(1) 实验室制备氨气的化学反应方程式为_________。
(2) 工业合成氨的反应方程式为:N2(g)+3H2(g) 2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。
2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。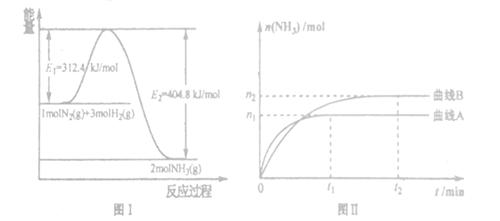
下列说法正确的是_______。
| A.ΔH=-92.4kJ/mol |
| B.使用催化剂会使E1的数值增大 |
| C.为了提高转化率,工业生产中反应的浓度越低越好 |
| D.图II是不同压强下反应体系中氨的物质的量与反应时间关系图,且PA<PB |
F.该反应的平銜常数KA<KB
G.在曲线A条件下,反应从开始到平衡,消耗N2的平均速率为
 mol/(L·min)
mol/(L·min)(3) —定温度下,向一个容积为2 L的密闭容器中通入2 mol N2和7 mol H2,达到平衡时测得容器的压强为起始时的
 倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______
倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______(4)已知H2(g)的燃烧热为285.8 kJ/mol,试写出表示NH3(g)燃烧热的热化学反应方程式_____。以氨气为燃料可以设计制氨燃料电池(电极材料均为惰性电极,KOH溶液作电解质溶液)该电池负极电极反应式为_______经測定,该电作过程中每放出1molN2实际提供460kJ的电能,则该燃料电池的实际效率为_____(燃料电池的实标效率是指电池实际提供的电能占燃料电池反应所能释放出的全部能量的百分数)
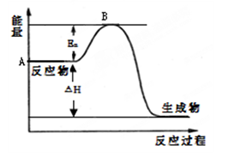
 2SO3(g),写出该反应的化学平衡常数表达式:
2SO3(g),写出该反应的化学平衡常数表达式: 
 CH3OH(g)+H2O(g) ΔH1 回答下列问题。
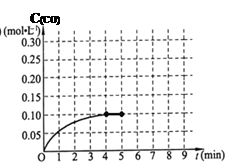
CH3OH(g)+H2O(g) ΔH1 回答下列问题。 CO(g) + 3H2(g),一定温度下,将2 mol CH4和4 mol H2O通入容积为10L的密闭反应室中,反应中CO的物质的量浓度的变化情况如图所示,请回答下列问题:
CO(g) + 3H2(g),一定温度下,将2 mol CH4和4 mol H2O通入容积为10L的密闭反应室中,反应中CO的物质的量浓度的变化情况如图所示,请回答下列问题: