��Ŀ����
����һ����Ҫ�Ļ�����Ʒ���ǵ��ʹ�ҵ���л��ϳɹ�ҵ�Լ��������ᡢ��κʹ����ԭ�ϣ�Ҳ��һ�ֳ��õ��������
(1) ʵ�����Ʊ������Ļ�ѧ��Ӧ����ʽΪ_________��
(2) ��ҵ�ϳɰ��ķ�Ӧ����ʽΪ��N2(g)��3H2(g) 2NH3(g) ��H����ͼI�Ǻϳɰ���Ӧ�������뷴Ӧ�������ͼ��δʹ�ô�������ͼD�Ǻϳɚݷ�Ӧ��2L�����С���ͬͶ������¡���������������ʱ��ijһ��Ӧ�����ĸı�Է�Ӧ��Ӱ��ͼ��
2NH3(g) ��H����ͼI�Ǻϳɰ���Ӧ�������뷴Ӧ�������ͼ��δʹ�ô�������ͼD�Ǻϳɚݷ�Ӧ��2L�����С���ͬͶ������¡���������������ʱ��ijһ��Ӧ�����ĸı�Է�Ӧ��Ӱ��ͼ��
����˵����ȷ����_______��
| A����H����92.4kJ/mol |
| B��ʹ�ô�����ʹE1����ֵ���� |
| C��Ϊ�����ת���ʣ���ҵ�����з�Ӧ��Ũ��Խ��Խ�� |
| D��ͼII�Dz�ͬѹǿ�·�Ӧ��ϵ�а������ʵ����뷴Ӧʱ���ϵͼ����PA<PB |
F.�÷�Ӧ��ƽ㕳���KA<KB
G.������A�����£���Ӧ�ӿ�ʼ��ƽ�⣬����N2��ƽ������Ϊ
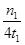 mol/(L��min)
mol/(L��min)(3) �����¶��£���һ���ݻ�Ϊ2 L���ܱ�������ͨ��2 mol N2��7 mol H2���ﵽƽ��ʱ���������ѹǿΪ��ʼʱ��
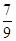 ��������¶��µ�ƽ�ⳣ��Ϊ_______����ͬһ�¶ȣ�ͬһ�����У�����ʼ���ʸ�Ϊamol N2 b molH2 c mol NH3 (a,b,c����Ϊ�㣩��ʹƽ�������и����ʵ�������ԭƽ����ͬ����a,b,c����Ĺ�ϵΪ_____________(�ú�a,b,c�ı���ʽ��ʾ��������ʹ��Ӧ����ʼʱ���淴Ӧ������У�c��ȡֵ��Χ��_______
��������¶��µ�ƽ�ⳣ��Ϊ_______����ͬһ�¶ȣ�ͬһ�����У�����ʼ���ʸ�Ϊamol N2 b molH2 c mol NH3 (a,b,c����Ϊ�㣩��ʹƽ�������и����ʵ�������ԭƽ����ͬ����a,b,c����Ĺ�ϵΪ_____________(�ú�a,b,c�ı���ʽ��ʾ��������ʹ��Ӧ����ʼʱ���淴Ӧ������У�c��ȡֵ��Χ��_______(4)��֪H2(g)��ȼ����Ϊ285.8 kJ/mol����д����ʾNH3(g)ȼ���ȵ��Ȼ�ѧ��Ӧ����ʽ_____������Ϊȼ�Ͽ�������ư�ȼ�ϵ�أ��缫���Ͼ�Ϊ���Ե缫,KOH��Һ���������Һ���õ�ظ����缫��ӦʽΪ_______���y�����õ���������ÿ�ų�1molN2ʵ���ṩ460kJ�ĵ��ܣ����ȼ�ϵ�ص�ʵ��Ч��Ϊ_____(ȼ�ϵ�ص�ʵ��Ч����ָ���ʵ���ṩ�ĵ���ռȼ�ϵ�ط�Ӧ�����ͷų���ȫ�������İٷ���)
��1��2NH4Cl��Ca(OH)2 CaCl2��2NH3����2H2O��2�֣� ��2��AEFG ��2�֣�
CaCl2��2NH3����2H2O��2�֣� ��2��AEFG ��2�֣�
��3��0.25L2��mol��2��2�֣�ƽ�ⳣ��������λҲ���֣���
a��0.5c��2��b��1.5c��7��2�֣���2��c��4��2�֣�
��4��NH3(g)��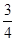 O2(g)��
O2(g)��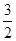 H2O(l)��
H2O(l)��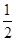 N2(g) ��H����382.5kJ/mol��2�֣�
N2(g) ��H����382.5kJ/mol��2�֣�
2NH3��6e����6OH����6H2O��N2��2�֣� 60.1%��1�֣�
�������������(1)ʵ�����Ʊ������Ļ�ѧ��Ӧ����ʽΪ2NH4Cl��Ca(OH)2 CaCl2��2NH3����2H2O��
CaCl2��2NH3����2H2O��
��2������ͼ��I��֪����Ӧ������������������������������˸÷�Ӧ�Ƿ��ȷ�Ӧ�����Ԧ�H��312.4kJ/mol=404.8kJ/mol����92.4kJ/mol��A��ȷ���������ͷ�Ӧ�Ļ�ܣ�����ʹ�ô�����ʹE1����ֵ����B����ȷ��Ϊ�����ת���ʣ���ҵ�����з�Ӧ��Ũ�Ȳ�����Խ��Խ�ã�C����ȷ������ͼ����֪������A���ȴﵽƽ��״̬����˵������A�ķ�Ӧ���ʿ졣��ƽ��ʱ����A��ʾ�İ������ʵ����ͣ���������Ӧ�������С�ķ��ȵĿ��淴Ӧ���������ߢ��б�ʾ�������������¶ȣ�����ѡ��D����ȷ��E��ȷ�������¶�ƽ�����淴Ӧ�����ƶ�������ƽ�ⳣ����С�����ѡ��F��ȷ������ͼ����֪����Ӧ���е�t1ʱ�����淴Ӧ�ﵽƽ��״̬����ʱ���ɰ��������ʵ�����n1mol���������ĵ��������ʵ�����2n1mol������������A�����£���Ӧ�ӿ�ʼ��ƽ�⣬����N2��ƽ������Ϊ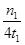 mol/(L��min)��G��ȷ����ѡAEFG��
mol/(L��min)��G��ȷ����ѡAEFG��
��3�� N2(g)��3H2(g) 2NH3(g)
2NH3(g)
��ʼŨ�ȣ�mol/L�� 1 3.5 0
ת��Ũ�ȣ�mol/L�� x 3x 2x
ƽ��Ũ�ȣ�mol/L�� 1��x 3.5��3x 2x
�ﵽƽ��ʱ���������ѹǿΪ��ʼʱ��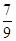 ��
��
����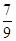 ��4.5��1��x��3.5��3x��2x
��4.5��1��x��3.5��3x��2x
���x��0.5
���Ը��¶��¿��淴Ӧ��ƽ�ⳣ��K��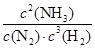 ��
�� ��0.25L2��mol��2
��0.25L2��mol��2
���ں��º����¶��ڷ�Ӧǰ��������������仯�ķ�Ӧ��˵������n��0����ϵ������Чת����Ӧ��������ʼͶ�ϵ����ʵ�����ԭƽ����ʼ̬��ͬ���ɣ��ݴ˿�֪��ʹƽ�������и����ʵ�������ԭƽ����ͬ����a,b,c����Ĺ�ϵΪa��0.5c��2��b��1.5c��7������ƽ��ʱ���������ʵ�����2mol������Ҫ��ʹ��Ӧ����ʼʱ���淴Ӧ������У�c��ȡֵ��Χ��c��2������ʼʱ��Ӧ������ʵ���Ϊ0ʱ�����������ʵ���������Ը���a��0.5c��2��b��1.5c��7��֪��c��4��4.7�����c��ȡֵ��Χ��2��c��4��
��3��H2(g)��ȼ����Ϊ285.8 kJ/mol��������ȼ�յ��Ȼ�ѧ����ʽ��H2(g)��0.5O2(g)��H2O(l) ��H����285.8 kJ/mol���٣����Ը���N2(g)��3H2(g) 2NH3(g) ��H����92.4kJ/mol���ڿ�֪���ڡ�2���١�
2NH3(g) ��H����92.4kJ/mol���ڿ�֪���ڡ�2���١�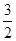 ���õ��Ȼ�ѧ����ʽNH3(g)��
���õ��Ȼ�ѧ����ʽNH3(g)��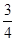 O2(g)��
O2(g)��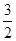 H2O(l)��
H2O(l)��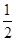 N2(g) ��H����382.5kJ/mol��ԭ��ظ���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ�������ڸ�ȼ�ϵ���а���ʧȥ���ӣ��ڸ���ͨ�룬��缫��Ӧʽ��2NH3��6e����6OH����6H2O��N2�����Ȼ�ѧ����ʽ��֪��ÿ����1molN2�ų�765kJ��������ʵ���ṩ460kJ�ĵ��ܣ����Ը�ȼ�ϵ�ص�ʵ��Ч��Ϊ
N2(g) ��H����382.5kJ/mol��ԭ��ظ���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ�������ڸ�ȼ�ϵ���а���ʧȥ���ӣ��ڸ���ͨ�룬��缫��Ӧʽ��2NH3��6e����6OH����6H2O��N2�����Ȼ�ѧ����ʽ��֪��ÿ����1molN2�ų�765kJ��������ʵ���ṩ460kJ�ĵ��ܣ����Ը�ȼ�ϵ�ص�ʵ��Ч��Ϊ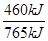 ��100%��60.1%��
��100%��60.1%��
���㣺���鰱���Ʊ�����Ӧ�ȡ���Ӧ���ʡ����������ƽ��״̬��Ӱ�졢��˹���ɵ�Ӧ�á�ƽ�ⳣ���ļ����Լ�ԭ���ԭ�����й�Ӧ�õ�

 Ŀ�����ϵ�д�
Ŀ�����ϵ�д��������ı仯�ͷ�Ӧ�Ŀ����ȽǶ��о���Ӧ��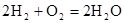 ��
��
��1��Ϊ�˼ӿ�����Ӧ���ʣ����Բ�ȡ�Ĵ�ʩ��________������ţ���ͬ����
| A��ʹ�ô��� | B���ʵ����������Ũ�� |
| C���ʵ���߷�Ӧ���¶� | D���ʵ����ͷ�Ӧ���¶� |
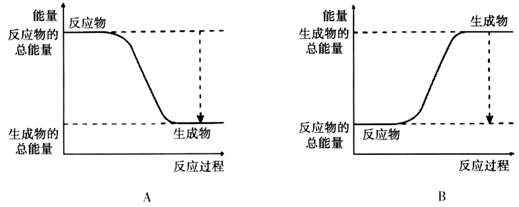
��3���Ӷϼ��ͳɼ��ĽǶȷ���������Ӧ�������ı仯��
�����ϡ��ټ��ܣ���1mol��ѧ����Ҫ���յ������������γ�1mol��ѧ�����ų���������Ϊ���ܡ�
�ڻ�ѧ���ļ��ܣ�
| ��ѧ�� | H��H | O��O | H��O |
����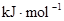 | 436 | 496 | 463 |
��������
| ��ѧ�� | ����������� �ų������� | �����仯 | |
| ��ѧ�� |  �еĻ�ѧ�� �еĻ�ѧ�� | _______________ | _______________ |
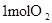 �еĻ�ѧ�� �еĻ�ѧ�� | |||
| �γɻ�ѧ�� | 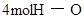 �� �� | _______________ | _______________ |
| �������仯 | _______________ | _______________ | |
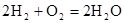 �����У�������________�������������������________��Ӧ�����������ԭ��������·��ÿת��0��2mol���ӣ���״��������H2�������________L��
�����У�������________�������������������________��Ӧ�����������ԭ��������·��ÿת��0��2mol���ӣ���״��������H2�������________L�� ���ǵ����Ϻ����ḻ��һ��Ԫ�أ���Ԫ�صĵ��ʺͻ������ڹ�ũҵ����������������Ҫ��;��
��1���������������仯ʾ��ͼ��
д��CO��NO2��Ӧ����NO��CO2���Ȼ�ѧ����ʽ
��2���ڹ̶�������ܱ������У��������»�ѧ��Ӧ��N2(g)+3H2(g)  2NH3 (g) ��H<0��
2NH3 (g) ��H<0��
��ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±������ж�K1 K2���>������=����<����
| T /K | 298 | 398 |
| ƽ�ⳣ��K | K1 | K2 |
��3�����и�����˵���÷�Ӧ�ﵽƽ��״̬���� ������ĸ��ţ�
a�� v(H2)��="3" v(N2)��
b�� ������ѹǿ���ֲ���
c�� �����л��������ܶȱ��ֲ���
d.�� N2��H2��NH3��Ũ��֮��Ϊ1:3:2
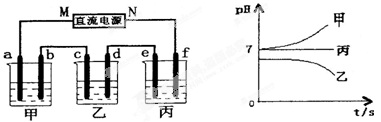
��4��������������ˮ,������ͼʵ������֤,�ڱ�״����,��ƿ�еİ�ˮʹ��̪��졣
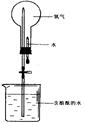
��ش�
���û�ѧ����˵�����ð�ˮ��ʹ��̪����ԭ�� ��
��250Cʱ����һ�����İ�ˮ�������Ϻ�pH=7����û����Һ��c(Cl-)��c(NH4+)��ϵΪ ������ĸ��ţ�
a��c(Cl-)��c(NH4+) b��c(Cl-)��c(NH4+)
c�� c(Cl-)��c(NH4+) d.���ж�
��15�֣�
�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ش�������״��йص����⣮
��1���״�������____���ӣ�����ԡ��Ǽ��ԡ�����
��2����ҵ��һ��ɲ������·�Ӧ���ϳɼ״���CO(g)+2H2(g) CH3OH(g)��H=-86.6kJ/mol����T��ʱ����һ������̶�Ϊ1L���ܱ������м���1mol CO��2mol H2������Ӧ�ﵽƽ��ʱ�������ڵ�ѹǿ�ǿ�ʼʱ��3/5��
CH3OH(g)��H=-86.6kJ/mol����T��ʱ����һ������̶�Ϊ1L���ܱ������м���1mol CO��2mol H2������Ӧ�ﵽƽ��ʱ�������ڵ�ѹǿ�ǿ�ʼʱ��3/5��
�ٴﵽƽ��ʱ��CO��ת����Ϊ ��
������ѡ�����жϸ÷�Ӧ�ﵽƽ��״̬�����ݵ���____ ��
A�� | B��CO���������ʵ���CH3OH���������� |
| C�������ڵ�ѹǿ���ֲ��� | D�����������ܶȱ��ֲ��� |
 ��3����֪�ڳ��³�ѹ�£�
��3����֪�ڳ��³�ѹ�£�
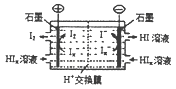
��4���ɼ״���������NaOH��Һ���ɵ������ֻ���أ���ʹ�ֻ�����ʹ��һ���²ų�һ�ε硣
�ٸõ�ظ����ĵ缫��ӦʽΪ____
�����Ըõ��Ϊ��Դ����ʯī���缫���200mL�����������ӵ���Һ��

���һ��ʱ��������ռ�����ͬ�������ͬ������������ʱ��������Һ����ı仯���缫������ܴ��ڵ��ܽ������������ռ�������������Ϊ ��
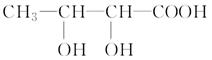
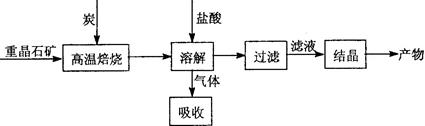
 4CO(g)+BaS(s) ��H1 = +571.2kJ/mol ��
4CO(g)+BaS(s) ��H1 = +571.2kJ/mol ��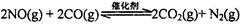 �����ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯���ߣ���ͼ��ʾ���ݴ��жϣ�
�����ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯���ߣ���ͼ��ʾ���ݴ��жϣ�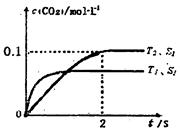
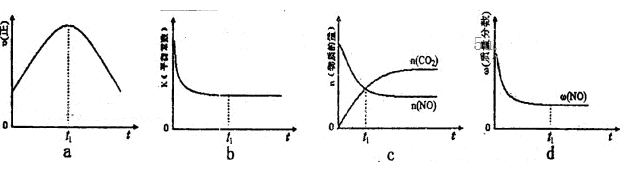
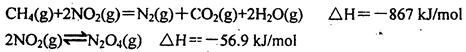
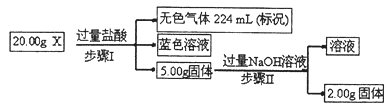
 N2(g)��CO2(g)ij�о�С��������ܱ���������һ�����Ļ���̿��NO�����£�T��C)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ������
N2(g)��CO2(g)ij�о�С��������ܱ���������һ�����Ļ���̿��NO�����£�T��C)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ������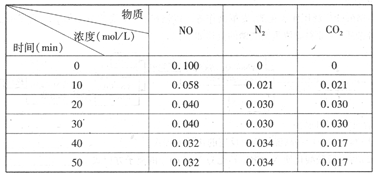
 N2��2CO2 ��H<0�о���������ʹ�õ���������ʱ����������ıȱ���������ѧ��Ӧ���ʣ�Ϊ�˷ֱ���֤�¶ȡ������ıȱ�����Ի�ѧ�� Ӧ���ʵ�Ӱ����ɡ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ������±��С�
N2��2CO2 ��H<0�о���������ʹ�õ���������ʱ����������ıȱ���������ѧ��Ӧ���ʣ�Ϊ�˷ֱ���֤�¶ȡ������ıȱ�����Ի�ѧ�� Ӧ���ʵ�Ӱ����ɡ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ������±��С�