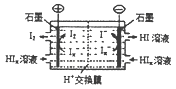
题目内容
已知:①溶液中CrO42—显黄色,Cr2O72-显橙红色
②PbCrO4难溶于水,也难溶于强酸
③H+(aq)+OH-(aq)=H2O(l); ΔH=" —a" KJ/mol
3Cl2(g)+2Cr3+(aq)+16OH-(aq)=2CrO42-(aq)+6Cl-(aq)+8H2O(l);ΔH="—b" KJ/mol
2CrO42-(aq)+2H+(aq)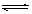 Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
平衡常数K=9.5×104 (上述a、b、c均大于0)
对上述反应⑤,取50mL溶液进行试验,部分测定数据如下:
| 时间(s) | 0 | 0.01 | 0.02 | 0.03 | 0.04 |
| n (CrO42—)(mol) | 0.01 | 8.0×10-4 | 5.4×10-4 | 5.0×10-4 | |
| n (Cr2O72—)(mol) | 0 | | 4.73×10-3 | | 4.75×10-3 |
试回答下列问题:
(1)0.02s到0.03s之间用Cr2O72-表示该反应的平均反应速率为
下列说法正确的( )
A、0.03s时V正(CrO42—)=2V逆(Cr2O72—)
B、溶液pH值不变说明该反应已达平衡状态
C、溶液中c(CrO42—):c(Cr2O72—)=2:1时该反应已达平衡状态
D、反应放热2.5×10-3c KJ时CrO42—的转化率为50%
E、升温该反应平衡常数变大
F、0.04s时加入足量的Pb(NO3)2 可使溶液由橙色变为黄色
(3)0.03s时溶液的pH=
(4)已知酸性条件下Cr2O72—将Cl-氧化为Cl2,本身被还原为Cr3+为放热反应,试写出该反应的热化学方程式:
(1)4×10-2mol/(L?S);(2)ABD;(3)1;
(4)Cr2O72- +6Cl-+14H+=3Cl2+2Cr3++7H2O ΔH=(c+b-16a)KJ/mol
解析试题分析:CrO42—的物质的量变化5.4×10-4- 5.0×10-4= 4.0×10-5 mol,用CrO42-表示的速率是8×10-2 mol/(L?S),依CrO42-(aq)+H+(aq) Cr2O72-可知,用Cr2O72—表示的速率是4×10-2 mol/(L?S) mol/(L?S)
Cr2O72-可知,用Cr2O72—表示的速率是4×10-2 mol/(L?S) mol/(L?S)
0.03s时,CrO42—有5.4×10-4- 5.0×10-4= 4.0×10-5 mol转变成Cr2O72—,Cr2O72—增加4.0×10-5 mol,即共为4.73×10-3+4.0×10-5 mol=4.75×10-3mol,所以0.03s时是平衡状态;此时V正(CrO42—)=2V逆(Cr2O72—)。A对。溶液pH值不变说明H+浓度不变,该反应已达平衡状态;B对。平衡是c(CrO42—):c(Cr2O72—)= 5.0×10-4: 4.75×10-3,不是2:1,C错。反应放热2.5×10-3c KJ时,CrO42—转化5.0×10-3 mol ,CrO42—的转化率为5.0×10-3 mol÷0.01mol =50%,D正确。该反应时放热反应,升温该反应平衡常数变小,E错误。0.04s时是平衡状态,由于PbCrO4难溶于水,也难溶于强酸,加入足量的Pb(NO3)2 可减小CrO42—浓度,使平衡左移,溶液由橙色变为黄色,最后为无色,F错误。平衡常数K=9.5×104 可以算出H+浓度是0.1mol/(L,pH= 1;(1)H+(aq)+OH-(aq)=H2O(l); ΔH=" —a" KJ/mol
(2)3Cl2(g)+2Cr3+(aq)+16OH-(aq)=2CrO42-(aq)+6Cl-(aq)+8H2O(l);ΔH="—b" KJ/mol
(3)2CrO42-(aq)+2H+(aq) Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol(1) ×16-(2)- (3)得:
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol(1) ×16-(2)- (3)得:
Cr2O72- +6Cl-+14H+=3Cl2+2Cr3++7H2O ΔH=(c+b-16a)KJ/mol
考点:反应速率、转化率、pH计算,平衡状态的判断,平衡常数分析,热化学方程式的书写。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案以下是一些物质的熔沸点数据(常压):
| | 钾 | 钠 | Na2CO3 | 金刚石 | 石墨 |
| 熔点(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 774 | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
金属钠和CO2在常压、890℃发生如下反应:4 Na(g)+ 3CO2(g)
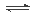 2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol(1)若反应在10L密闭容器、常压下进行,温度由890℃升高到1860℃,若反应时间为10min, 金属钠的物质的量减少了0.2mol,则10min内CO2的平均反应速率为 。
(2)高压下有利于金刚石的制备,理由是 。
(3)由CO2(g)+ 4Na(g)=2Na2O(s)+ C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
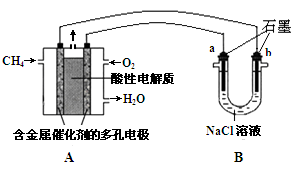
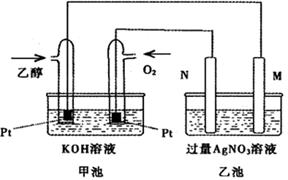
(4)下图开关K接M时,石墨电极反应式为 。
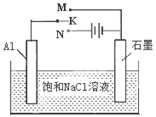
(5)请运用原电池原理设计实验,验证Cu2+、Ag+氧化性的强弱。
在方框内画出实验装置图,要求用烧杯和盐桥(在同一烧杯中,
电极与溶液含相同的金属元素),并标出外电路电子流向。
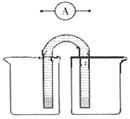
实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
⑴已知某反应的平衡表达式为:
它所对应的化学反应方程式为:
⑵利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g);ΔH=-90.8kJ·mol
CH3OH(g);ΔH=-90.8kJ·mol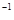
②2CH3OH(g) CH3OCH3(g)+H2O(g);ΔH=-23.5kJ·mol
CH3OCH3(g)+H2O(g);ΔH=-23.5kJ·mol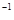
③CO(g)+H2O(g) CO2(g)+H2(g);ΔH=-41.3kJ·mol
CO2(g)+H2(g);ΔH=-41.3kJ·mol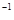
总反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的ΔH=__________
CH3OCH3(g)+CO2(g)的ΔH=__________
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
该反应的正反应方向是反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为:。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。
对反应:N2O4(g)
 2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是。
2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是。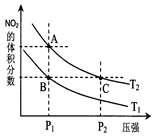
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
E.A、C两点的化学平衡常数:A>C
(5)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。下列说法正确的是
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。下列说法正确的是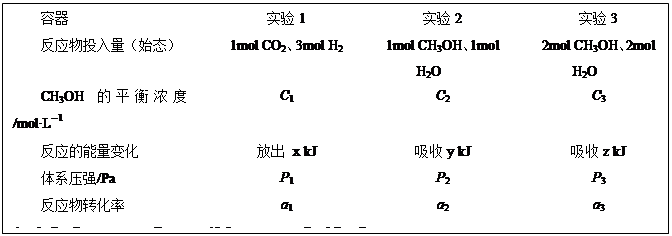
 CH3OCH3+H2O
CH3OCH3+H2O CH3OCH3(g)+CO2(g) △H=-247kJ/mol
CH3OCH3(g)+CO2(g) △H=-247kJ/mol


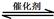 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
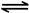 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol