题目内容
下列各图与表述不一致的是
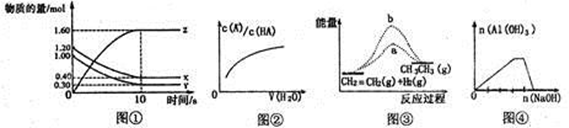

| A.图①表示T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线。若T℃时,若起始时X为1.20mol,Y为1.00mol,则平衡时Y的转化率为80% |
| B.图②中曲线表示向弱酸HA的稀溶液中加水稀释 |
| C.图③b曲线表示反应CH2=CH2(g)+H2(g)→CH3-CH3(g) △H<0,使用催化剂时,反应过程中的能量变化 |
| D.图④表示向NH4Al(SO4)2溶液中滴加过量的NaOH溶液 |
C
图①中起始时Y为1.00mol,平衡是Y为0.20mol,故平衡时Y的转化率为80%,A正确;加水稀释,HA的电离程度增大,溶液中n(A-)增大,n(HA)减小,故图②中随着加入水的量增加,c(A-)/c(HA)逐渐增大,B正确;使用催化剂后,反应活化能降低,故图③中曲线a表示使用催化剂时反应过程中的能量变化,C错误;向NH4Al(SO4)2溶液中滴加过量的NaOH溶液的过程中,依次发生的反应:Al3++3OH-= Al(OH)3↓,NH4++OH-=NH3·H2O,Al(OH)3+OH-="[" Al(OH)4]-,图④与反应过程一致,D正确。

练习册系列答案
相关题目
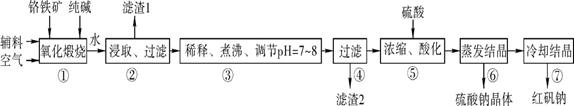
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2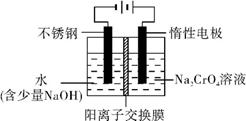
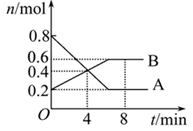
 2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。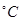 时,在2L的恒容密闭容器中充入2molNO和1molO2发生反应,2NO(g)+O2(g)
时,在2L的恒容密闭容器中充入2molNO和1molO2发生反应,2NO(g)+O2(g) 2NO2(g),经5min达到平衡,测得c(NO)="0.5" mol/L,并放热QkJ。5min内 v(O2)=___________。
2NO2(g),经5min达到平衡,测得c(NO)="0.5" mol/L,并放热QkJ。5min内 v(O2)=___________。
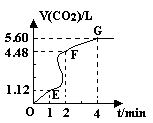 (气体体积均在标准状况下测定)。请回答下列问题:
(气体体积均在标准状况下测定)。请回答下列问题: (3)加入CaCO3的质量为 。
(3)加入CaCO3的质量为 。 SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某温度时向体积为1 L的恒容密闭容器中充入0. 20mol SO2Cl2,达到平衡时,容器中含0.18mol SO2,则此过程反应吸收的热量为_____ kJ,该温度时反应的平衡常数为_____。将上述所得混合气体溶于足量BaCl2溶液中,最终生成沉淀的质量为_______。
SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某温度时向体积为1 L的恒容密闭容器中充入0. 20mol SO2Cl2,达到平衡时,容器中含0.18mol SO2,则此过程反应吸收的热量为_____ kJ,该温度时反应的平衡常数为_____。将上述所得混合气体溶于足量BaCl2溶液中,最终生成沉淀的质量为_______。
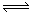 xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )
xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是( )