题目内容
(12分)在一容积为2L的密闭容器中加入2molA和6molB,保持温度为20℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)  2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
⑴求20℃时,该反应的平衡常数K(保留三位有效数字)
⑵20℃时,若在同一容器中加入1molA、 mol B和 mol C,则平衡混合气中C的体积分数仍为ω。
 2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。⑴求20℃时,该反应的平衡常数K(保留三位有效数字)
⑵20℃时,若在同一容器中加入1molA、 mol B和 mol C,则平衡混合气中C的体积分数仍为ω。
⑴ 0.0893 ⑵4molB 2mol C
试题分析:(1)在反应达到平衡时由于产生C1.2mol,根据方程式可知消耗的A、B的物质的量分别是0.6mol、1.2mol。因此平衡时各种物质的浓度是:c(A)=(2-0.6)mol÷2L=0.7mol/L;c(B)=(6-1.2)mol÷2L=2.4mol/L;c(A)=1.2mol÷2L=0.6mol/L。因此20℃时,该反应的平衡常数
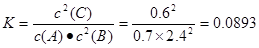 。⑵在恒温恒容条件下,对于反应前后气体体积不同的可逆反应,若一边倒转化后气体的物质的量相同,则平衡时等效。平衡混合气中C的体积分数仍为ω。假设要加入B、C的物质的量分别是x、y.可以认为ymol的C不是加入的而是反应消耗A、B产生的,则根据方程式中的关系可知反应消耗A:y/2mol;B:ymol。则开始时加入的A为(1+ y/2)mol;加入的B为(x+ y)mol。所以1+ y/2=2;x+ y=6.解得x=4;y=2..即开始时加入1mol的A;4molB;2mol的C。
。⑵在恒温恒容条件下,对于反应前后气体体积不同的可逆反应,若一边倒转化后气体的物质的量相同,则平衡时等效。平衡混合气中C的体积分数仍为ω。假设要加入B、C的物质的量分别是x、y.可以认为ymol的C不是加入的而是反应消耗A、B产生的,则根据方程式中的关系可知反应消耗A:y/2mol;B:ymol。则开始时加入的A为(1+ y/2)mol;加入的B为(x+ y)mol。所以1+ y/2=2;x+ y=6.解得x=4;y=2..即开始时加入1mol的A;4molB;2mol的C。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
 2HF(g) ΔH>0,且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) ΔH>0,且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是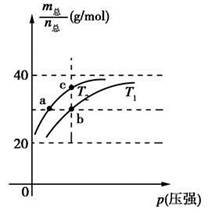
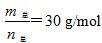 时,n(HF):n[(HF)2]=2:1
时,n(HF):n[(HF)2]=2:1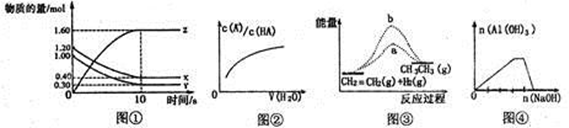
 Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是( )
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是( ) p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为