题目内容
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定,下列实验中用高锰酸钾与浓盐酸反应制备得到氯气,然后再将氯气通入氢氧化钾溶液中与氢氧化铁固体充分反应而制得产品:
(1)制备K2FeO4(夹持装置略)
①请写出该过程中制备氯气的离子反应方程式________________(锰被还原为Mn2+)。
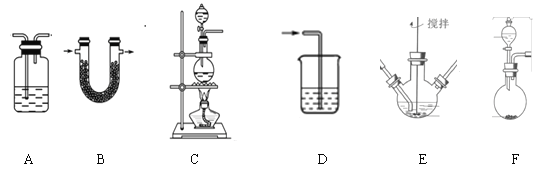
②请根据高铁酸钾制备的原理选择合适的装置,连接顺序为_________→ E →_________。(上述装置不一定全部用到,装置可以重复选用)
③装置E中反应时需进行搅拌,目的是_______________________
④E中得到紫色固体和溶液。E中生成高铁酸钾的反应为______________;反应充分进行后,E中溶液中主要的阴离子为__________________
(2)探究K2FeO4的性质
取E中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否是K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤E中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
②方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________
【答案】2MnO4- + 16H+ + 10Cl- =2Mn2+ +5Cl2↑+8H2O; F A D 使反应物氯气和固体氢氧化铁能充分接触,加快反应速率,提高产率。 3Cl2 + 2Fe(OH)3 + 10KOH = 2K2FeO4 + 6KCl + 8H2O Cl-,ClO-,OH-,FeO42- Fe3+ 4FeO42 + 20H+ = 4Fe3+ + 3O2↑ + 10H2O 避免ClO干扰实验。
【解析】
(1)①用高锰酸钾和浓盐酸反应制取Cl2,MnO4被还原为Mn2+,Cl被氧化为Cl2,据此写出反应的离子方程式;
②高锰酸钾和浓盐酸反应制取Cl2不需要加热,因此选用F装置,浓盐酸会挥发产生HCl,使得产生的Cl2中混有HCl,需要除去HCl,可将混合气体通过饱和食盐水达到除杂的目的,选用装置A,除去HCl的Cl2进入装置E发生反应制备高铁酸钾,最后连接D装置进行尾气吸收;
③搅拌能使反应物氯气和固体氢氧化铁充分接触,加快反应速率,提高产率;
④E中得到紫色固体和溶液,紫色固体为K2FeO4,在碱性条件下,Cl2可以氧化Fe(OH)3制取K2FeO4,据此写出反应方程式,同时还存在反应为Cl2和KOH反应,据此判断溶液中的阴离子;
(2)①方案I中加入KSCN溶液至过量,溶液呈红色,说明反应产生Fe3+,但该离子的产生不能判断一定是K2FeO4将Cl氧化,注意K2FeO4在碱性溶液中稳定,酸性溶液中快速产生O2,自身转化为Fe3+;
②方案II可证明K2FeO4氧化了Cl,使用KOH溶液溶出K2FeO4晶体,可以使K2FeO4稳定析出,并且除去ClO离子,防止在酸性条件下ClO和Cl反应产生Cl2干扰实验。
(1)①用高锰酸钾和浓盐酸反应制取Cl2,MnO4被还原为Mn2+,Cl被氧化为Cl2,据此写出反应的离子方程式:2MnO4-+16H++10Cl-=2Mn2+ +5Cl2↑+8H2O;
故答案为:2MnO4-+16H++10Cl-=2Mn2+ ++5Cl2↑+8H2O;
②高锰酸钾和浓盐酸反应制取Cl2不需要加热,因此选用F装置,浓盐酸会挥发产生HCl,使得产生的Cl2中混有HCl,需要除去HCl,可将混合气体通过盛有饱和食盐水的洗气瓶达到除杂的目的,选用装置A,除去HCl的Cl2进入装置E发生反应制备高铁酸钾,最后连接D装置进行尾气吸收;
故答案为:F A;D;
③搅拌能使反应物氯气和固体氢氧化铁充分接触,加快反应速率,提高产率;
故答案为:使反应物氯气和固体氢氧化铁能充分接触,加快反应速率,提高产率;
④E中得到紫色固体和溶液,紫色固体为K2FeO4,在碱性条件下,Cl2可以氧化Fe(OH)3制取K2FeO4,反应方程式为:3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,同时还存在反应为Cl2和KOH反应:Cl2 + 2KOH= KCl + KClO + H2O,因此E溶液中主要的阴离子为Cl-,ClO-,OH-,FeO42-;
故答案为:3Cl2 + 2Fe(OH)3 + 10KOH = 2K2FeO4 + 6KCl + 8H2O; Cl-,ClO-,OH-,FeO42-。
(2)①方案I中加入KSCN溶液至过量,溶液呈红色,说明反应产生Fe3+,但该离子的产生不能判断一定是K2FeO4将Cl氧化,注意K2FeO4在碱性溶液中稳定,酸性溶液中快速产生O2,自身转化为Fe3+,反应为4FeO42+20H+=4Fe3++3O2↑+10H2O;
故答案为:Fe3+;4FeO42 + 20H+ = 4Fe3+ + 3O2↑ + 10H2O;
②方案II可证明K2FeO4氧化了Cl, 使用KOH溶液溶出K2FeO4晶体,可以使K2FeO4稳定析出,同时考虑到K2FeO4表面可能吸附ClO,ClO在酸性条件下可与Cl反应生成Cl2,从而干扰实验,所以用KOH溶液洗涤的目的是:避免ClO干扰实验;
故答案为:避免ClO干扰实验。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案