题目内容
【题目】铁、铝、铜等金属及其化合物在日常生活中应用广泛,请回答下列问题。
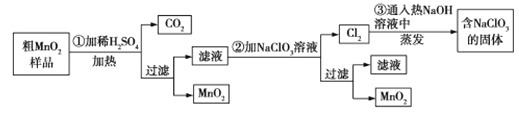
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸,离子方程式为_______________________________________________________;Y与过量浓硝酸反应后溶液中含有的盐的化学式为____________;
(2)某溶液中含有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填编号)。
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
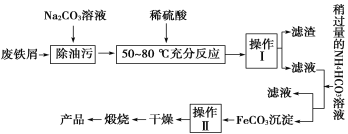
①Na2CO3溶液可以除油污,原因是(用离子方程式表示)________________________________;
②操作Ⅱ中沉淀的洗涤方法是___________________________________________________________
③请写出生成FeCO3沉淀的离子方程式_______________________________________________。
【答案】Fe3O4+8H+===2Fe3++Fe2++4H2O Fe(NO3)3BCCO32-+H2O![]() HCO3-+OH-向漏斗中加入蒸馏水至没过固体,让水自然流出,重复2~3次Fe2++2HCO3-=FeCO3↓+CO2↑+H2O
HCO3-+OH-向漏斗中加入蒸馏水至没过固体,让水自然流出,重复2~3次Fe2++2HCO3-=FeCO3↓+CO2↑+H2O
【解析】
(1)Fe3C在足量的空气中高温煅烧,生成有磁性的固体Y,Y为Fe3O4,溶于过量的盐酸反应生成氯化亚铁、氯化铁,化学反应方程式为Fe3O4+8HCl==2FeCl3+FeCl2+4H2O,硝酸具有强氧化性,Fe3O4与过量的浓硝酸反应生成硝酸铁,化学式为Fe(NO3)3;
(2)加入过量的NaOH,Al3+转化为偏铝酸根,Mg2+、Fe2+、Cu2+转化为氢氧化物沉淀,且氢氧化亚铁易被氧化,灼烧固体得到氧化镁、氧化铜、氧化铁,用过量的稀盐酸中,所得溶液中含有Mg2+、Fe3+、Cu2+,与原溶液相比,溶液中大量减少的阳离子是Al3+、Fe2+,故选BC;
(3)①碳酸钠溶液中碳酸根水解CO32-+H2OHCO3-+OH-,溶液呈碱性,油污主要为油脂,碱性条件下水解而除去;②FeCO3沉淀会附着其它离子,需要进行洗涤,减少杂质,具体操作为:向漏斗中加入蒸馏水至没过固体,让水自然流出,重复2~3次;③由工艺流程可知,操作I所得的滤液中主要有硫酸亚铁,加入碳酸氢铵,实质是亚铁离子与碳酸氢根离子反应,生成FeCO3, 同时生成二氧化碳、水,反应离子方程式为:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】根据下列短周期元素性质的数据判断,下列说法正确的是( )
|
|
|
|
|
|
|
| |
原子半径 |
|
|
|
|
|
|
|
|
最高价或最低价 |
|
|
|
|
|
|
|
|
A. 元素④⑤形成的化合物是离子化合物
B. 元素⑦位于第二周期第V族
C. 元素①⑧形成的化合物具有两性
D. 元素③的最高价氧化物对应水化物的碱性最强