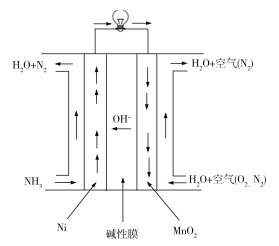
题目内容
【题目】在一定温度和体积固定的密闭容器中,可逆反应H2(g)+I2(g) ![]() 2HI(g) (无色)达平衡状态,该状态下,说法不正确的是( )
2HI(g) (无色)达平衡状态,该状态下,说法不正确的是( )
A. 可逆反应停止 B. I2浓度不再变化
C. HI浓度不再变化 D. 混合气体颜色不再变化
【答案】A
【解析】
A.可逆反应达到平衡状态时正逆反应速率相等但不等于0,反应也没有停止,是一个动态平衡,故A错误;
B. 在一定条件下,反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,平衡时I2浓度不再发生变化,说明达到平衡状态,故B正确;
C.在一定条件下,反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,平衡时HI浓度不再发生变化,说明达到平衡状态,故C正确;
D.在反应混合物中I2(g)是紫色气体,其它都是无色气体。如果反应未达到平衡,则I2(g)的浓度就要发生变化,混合气体的颜色就要改变。若反应达到平衡,则气体的颜色就不会发生变化。因此混合气体的颜色不再改变能作为判断反应达到平衡的标志,故D正确。
故选D。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。所发生的转化过程为CH3CH2CH2CH2OH![]() CH3CH2CH2CHO。
CH3CH2CH2CHO。

反应物和产物的相关物理性质如表所示。
性质 | 沸点/℃ | 密度/g·cm-3 | 水中溶解性 |
正丁醇 | 117.2 | 0.810 9 | 微溶 |
正丁醛 | 75.7 | 0.801 7 | 微溶 |
实验步骤如下:
将6.0g Na2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分。将馏出物倒入分液漏斗中,分去水层,将有机层干燥后蒸馏,收集75~77℃馏分,产量为2.0 g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加入浓硫酸中,说明理由:___________。
(2)加入沸石的作用是___________,若加热后发现未加入沸石,应采取的正确措施是___________。
(3)上述装置图中,B仪器的名称是____,D仪器的名称是_______。
(4)将正丁醛粗产品置于分液漏斗中分离水时,水在______(填“上”或“下”)层。
(5)反应温度应保持在90~95℃,其原因是______________________。
(6)本实验中,正丁醛的产率为_____%。
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定,下列实验中用高锰酸钾与浓盐酸反应制备得到氯气,然后再将氯气通入氢氧化钾溶液中与氢氧化铁固体充分反应而制得产品:
(1)制备K2FeO4(夹持装置略)
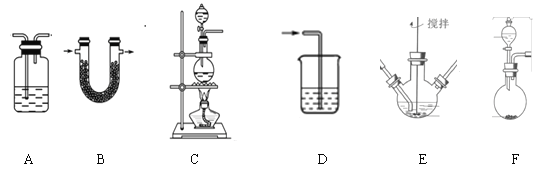
①请写出该过程中制备氯气的离子反应方程式________________(锰被还原为Mn2+)。
②请根据高铁酸钾制备的原理选择合适的装置,连接顺序为_________→ E →_________。(上述装置不一定全部用到,装置可以重复选用)
③装置E中反应时需进行搅拌,目的是_______________________
④E中得到紫色固体和溶液。E中生成高铁酸钾的反应为______________;反应充分进行后,E中溶液中主要的阴离子为__________________
(2)探究K2FeO4的性质
取E中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否是K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤E中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
②方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________